IF:6.7/Q1,多组学+网络药理学方法揭示龟龄集通过调节花生四烯酸途径缓解少弱畸形精子症!!!
题目:多组学和网络药理学方法揭示龟龄集通过调节花生四烯酸途径缓解少弱畸形精子症
英文名:Multi-omics and network pharmacology approaches reveal Gui-Ling-Ji alleviates oligoasthenoteratozoospermia by regulating arachidonic acid pathway
杂志:Phytomedicine
影响因子:6.7/Q1
发表时间:2024年10月
研究背景: 龟龄集(GLJ)是一种用于提高男性生育能力的传统中药配方。 少弱畸形精子症(OAT)是导致男性不育的最重要原因之一。龟龄集现在可用于治疗少弱畸形精子症(OAT)。然而,GLJ的活性成分和机制尚不清楚。
研究思路:首先,建立环磷酰胺 (CTX)诱导的OAT大鼠模型,评价GLJ的疗效。其次,进行基于血清/尿液的代谢组学和脂质组学和基于组织的转录组学,以发现大鼠的差异代谢物和基因。此外,基于多组学分析结果构建网络药理学以探索相关机制。最后,使用睾丸间充质基质细胞(TM3)的细胞实验来验证活性成分和关键代谢途径。

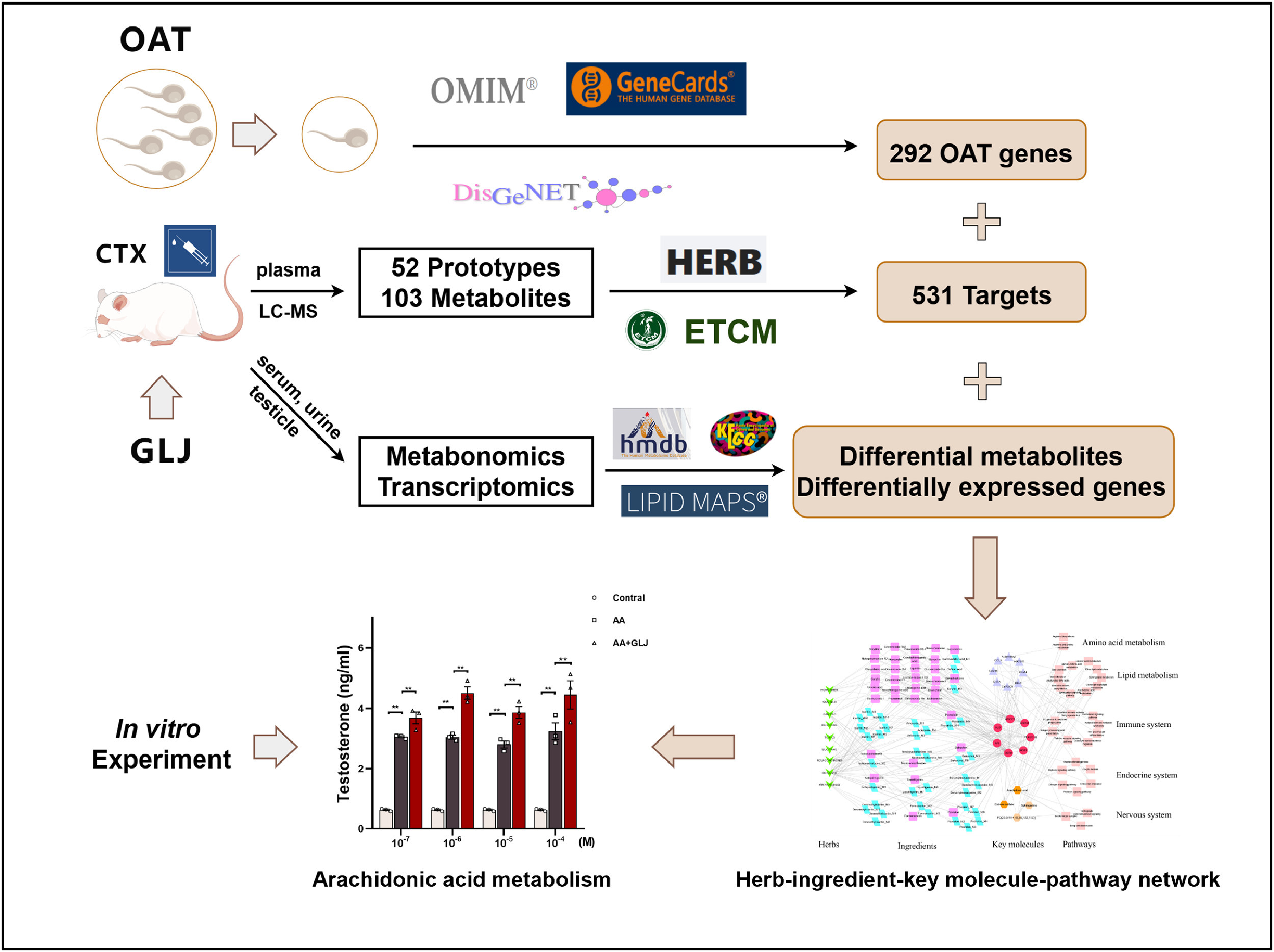
图1
研究结果:
1、GLJ可提高大鼠的精子活力并调节血清中的性激素水平
为了评估GLJ的疗效,在动物实验期间,每天都对所有大鼠进行称重,并观察它们的身体状况。在给药前的第1天至第14天,各组大鼠的体重差异无统计学意义。此外,GLJ-L组和GLJ-H组大鼠的毛色、精神状态和摄食状况均正常。本研究采用六磷酸肌醇(IP6)作为阳性对照药物。IP组大鼠的精子数量和活性是OAT组大鼠的1.5倍。如图2A所示,GLJ能有效减缓CTX引起的体重下降,在CTX进行OAT造模后的第15至17天,OAT大鼠的体重明显下降,而GLJ-L组和GLJ-H组大鼠的体重下降速度明显慢于OAT造模组。附睾中的精液是OAT最直观的指标,对其进行了检测和分析。图2(B和C)显示,OAT大鼠的精子数量和活力明显减少,而GLJ大鼠的精子数量和活力则明显增加。此外,OAT大鼠血清中的黄体生成素(LH)、卵泡刺激素(FSH)和睾酮(T)水平明显降低,但使用GLJ治疗后有所改善(图2D-F)。如睾丸切片HE染色(图2G-I)所示,OAT组(OAT vs. Sham)的曲细精管形态紊乱,管腔内的生精细胞数量明显减少。随后,OAT大鼠的曲细精管萎缩和生精细胞数量的减少在使用GLJ-H治疗后得到缓解。
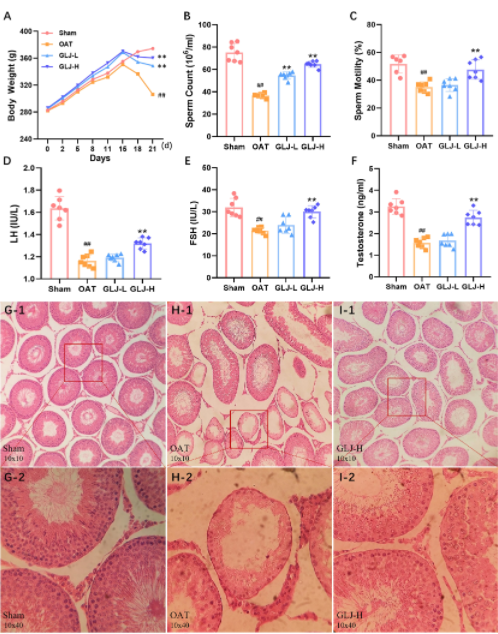

图2
2、大鼠血清和尿液的代谢组学和脂质组学分析
通过分析OAT和GLJ引起的内源性差异代谢物(DMs),在尿液和血清样本中分别鉴定出106种和85种内源性DMs,这些DMs在两组之间的分布如图3(A和B)所示。
此外,还绘制了反映体内含量变化的热图。如图3(D和E)所示,代谢组学确定的88种DM(尿液中有37种DM,血清中有51种DM)受GLJ调节。血清样本中65%受调控的代谢物是脂质代谢物。因此,对血清进行了脂质组分析,确定了159种脂质DMs(图3C),54种受GLJ调控的DMs的热图结果见图3F,其中包括33%的甘油磷脂、20%的甘油脂类、17%的类固醇、6%的鞘脂类等。在这些DM中,OAT组的AA水平明显高于Sham组,而GLJ-L组和GLJ-H组则明显低于OAT组。同时,与AA相关的脂质DMs(即PGE2、PGE2a、白三烯E4、12-HETE)在GLJ-L组和GLJ-H组明显升高。

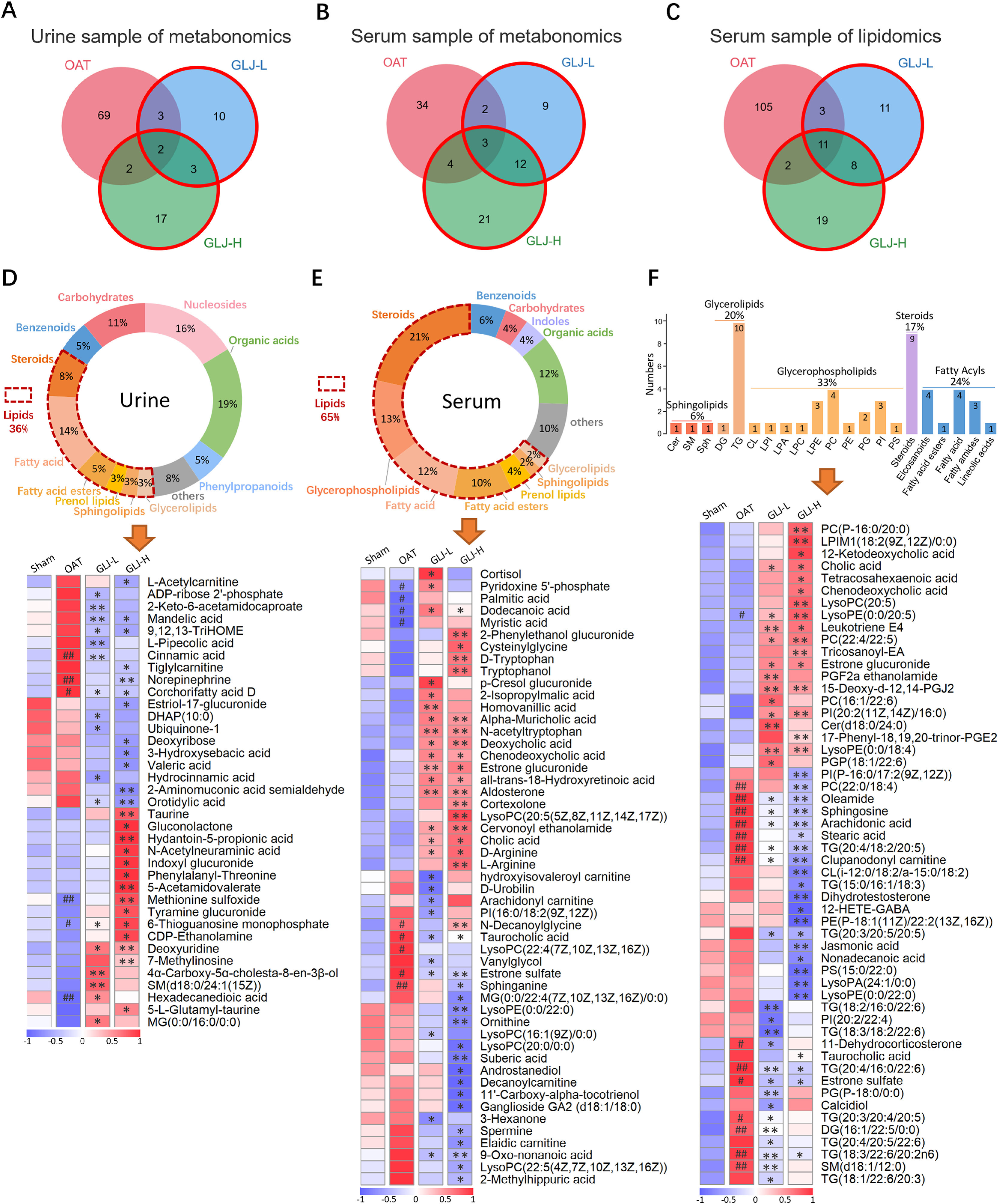
图3
3、DM的功能分析
图4A显示,鞘脂代谢在所有3组的DMs中都富集,而甘油磷脂代谢和不饱和脂肪酸生物合成的通路在OAT vs. Sham组或GLJvs.OAT组的DMs中富集。发现了四条通路,包括鞘脂代谢、花生四烯酸代谢、甘油磷脂代谢和醚脂代谢(图4B)。接着,由四条途径和与途径相关的DMs组成的四个连接模块构成了一个代谢物-途径网络(图4C)。该网络中的8个DMs在OAT组和GLJ组中有相反的表达(图4D),其中7个代谢物在OAT处理后增加,而在GLJ处理后则下调,尤其是花生四烯酸和鞘磷脂。在OAT组和Sham组中,有3条途径被富集(图4E),其中DM在11条途径中发挥了关键作用(图4F)。对包括5个连接模块的DMs途径网络进行了分析(图4G),在该网络中,只有一种代谢物在OAT组与Sham组和GLJ组与OAT组中有相反的表达。如图4H所示,去甲肾上腺素在OAT组中增加,而在GLJ-L组中减少。GLJ可能通过调节去甲肾上腺素来提高男性生育能力。

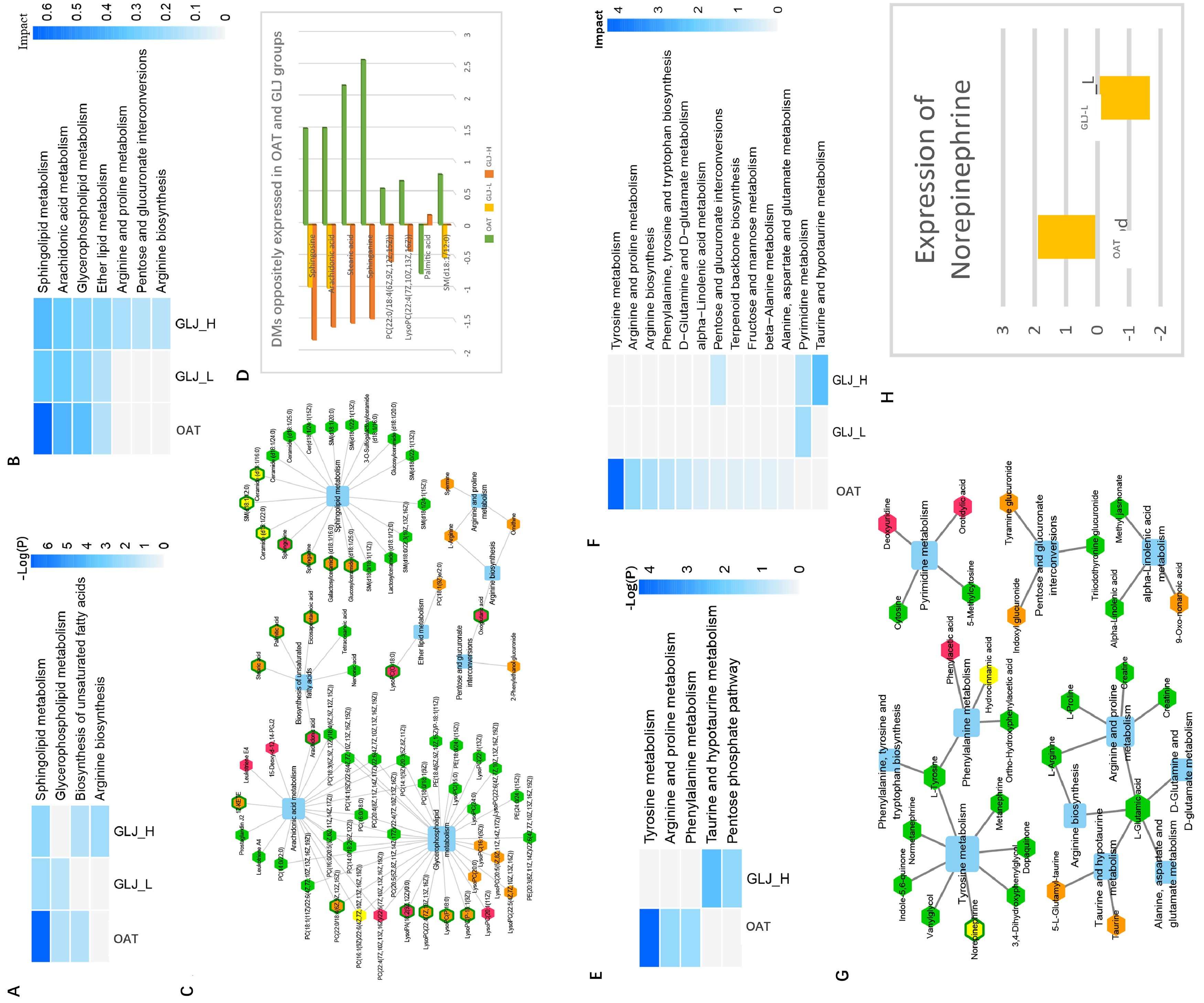
图4
4、大鼠睾丸差异表达基因的鉴定和功能分析
为了阐明GLJ治疗大鼠与未治疗大鼠之间基因转录水平的变化,对差异表达基因进行了分析,最终确定了305个DEGs。将OAT组与Sham组和GLJ组与OAT组中相反表达的23个DEGs(图5a和B)输入STRING进行功能注释,发现这些基因富集了3个通路,这些通路与免疫和内分泌系统的生物过程有关。并进行了GO、KEGG分析(图5C-E)。
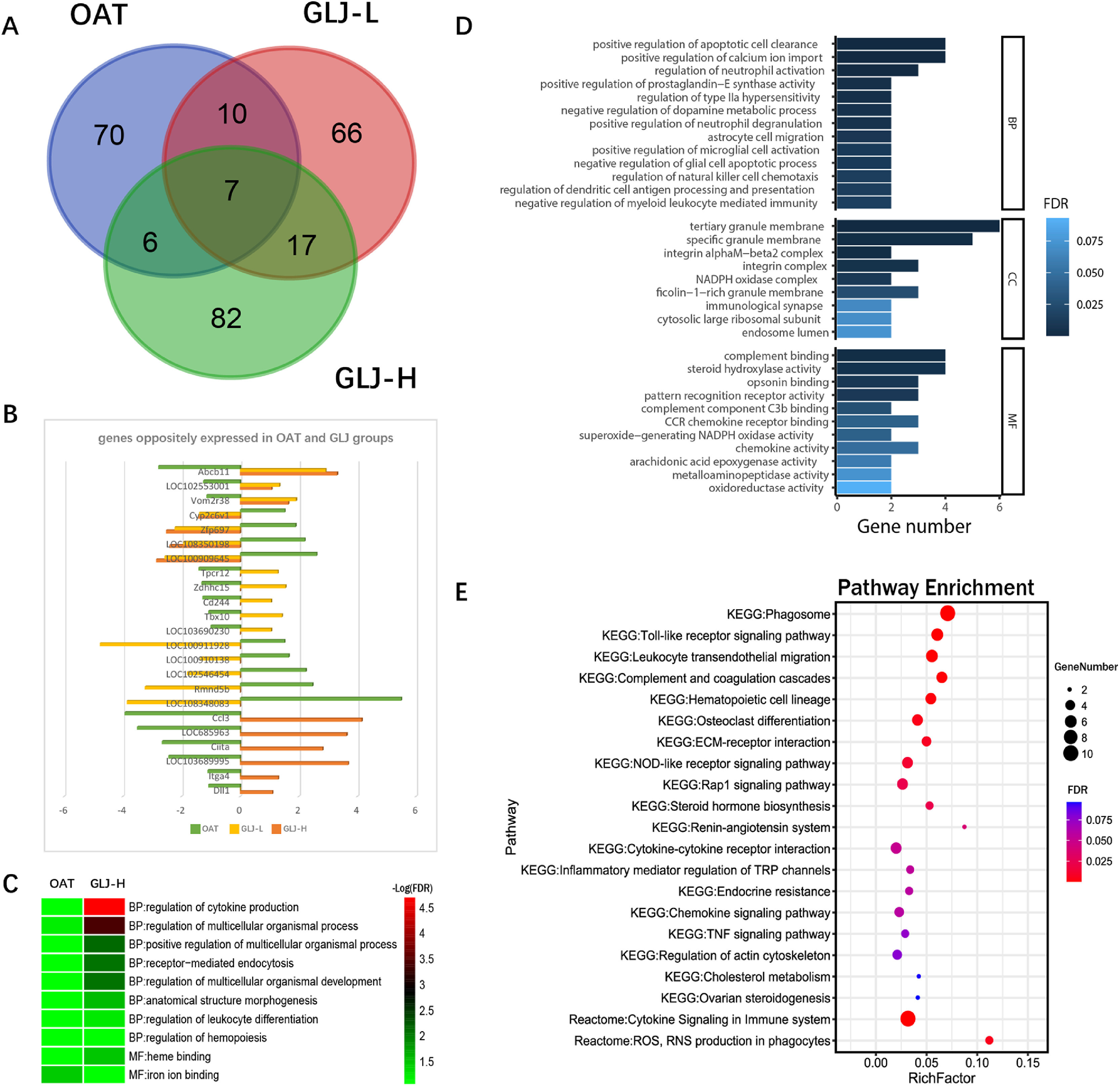
图5
5、多组学结果和GLJ潜在靶标的综合网络分析
利用网络药理学技术对代谢组学、脂质组学和转录组学数据进行了综合分析,得到GLJ基因-代谢物网络(图6A)。筛选确定了前30条通路(图6B),包括内分泌系统、免疫系统和脂质代谢(内分泌抵抗、T细胞受体信号通路和类固醇激素生物合成等)。构建GLJ基因-DM网络,分析DM与OAT中GLJ的治疗密切相关的调控基因(图6C-D)。然后,将目标得分定义为药材与药材配对的数量。12个重要靶标的靶向得分如图6E所示。建立了"药材-成分-关键分子-途径"网络(图6F)。在19个关键靶点中,花生四烯酸是网络中最重要的代谢物节点。因此,预计花生四烯酸代谢在GLJ治疗OAT的过程中具有关键作用。
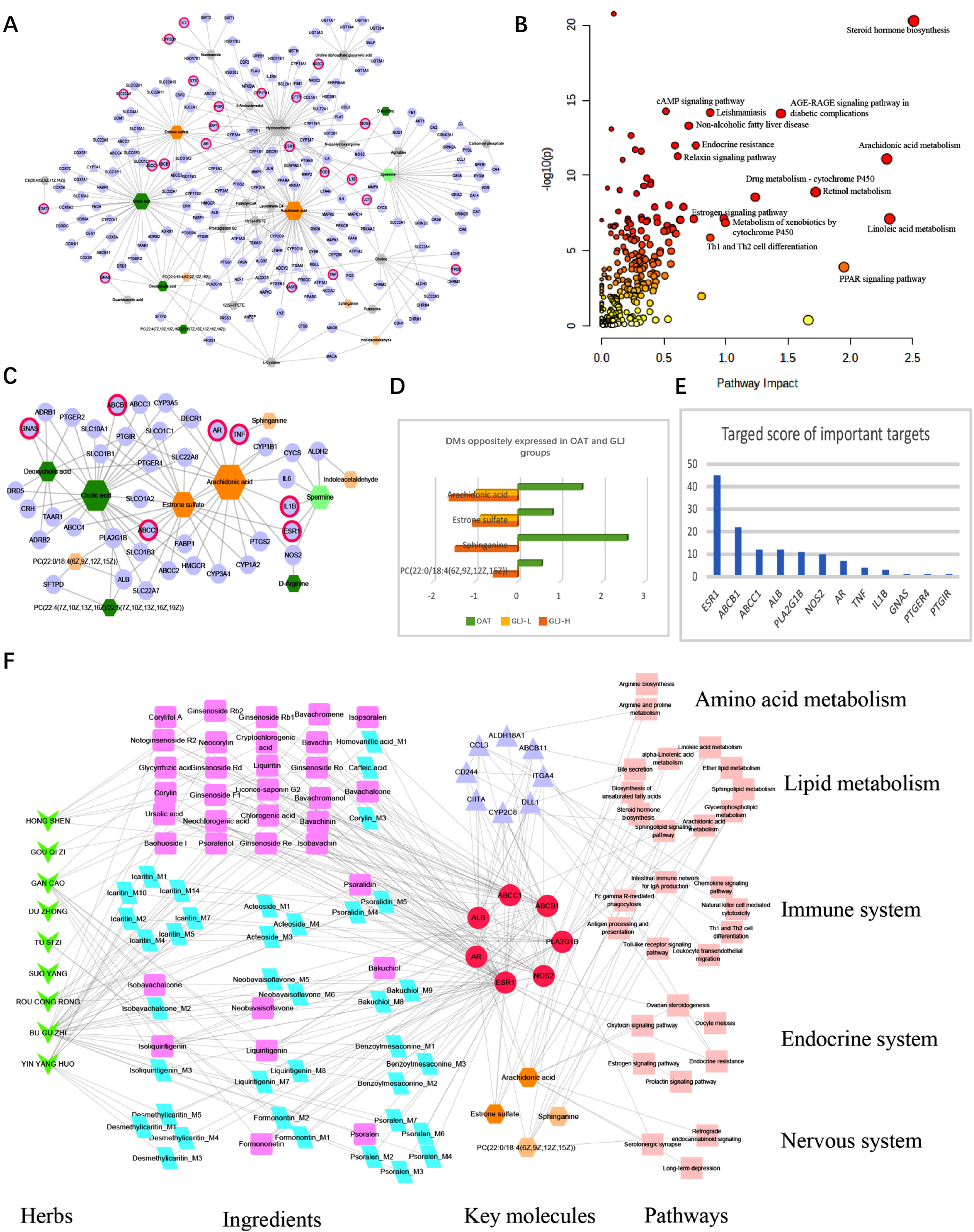

图6
6、GLJ及其成分对睾酮分泌的影响
如图7(A-F)所示,GLJ以浓度依赖性的方式显著提高了睾酮分泌水平。在所测试的八种化合物中,发现补骨脂素(psoralen)对睾酮分泌的影响maximum,在5μM时就能显著增强睾酮分泌,而异甘草苷(isoliquiritin)、人参皂苷Ro(ginsenoside Ro)、甘草素(liquiritigenin)和异补骨脂素(isopsoralen)也能显著提高T水平(在25μM时,T水平highest可达0.448±0.041ng/mL)。至于淫羊藿苷(liquiritin)、异补骨脂素(icariin)和熊果酸( ursolic acid),淫羊藿苷(liquiritin)对T水平的影响有限,而异补骨脂素(icariin)和熊果酸( ursolic acid)对TM3具有抗增殖特性。
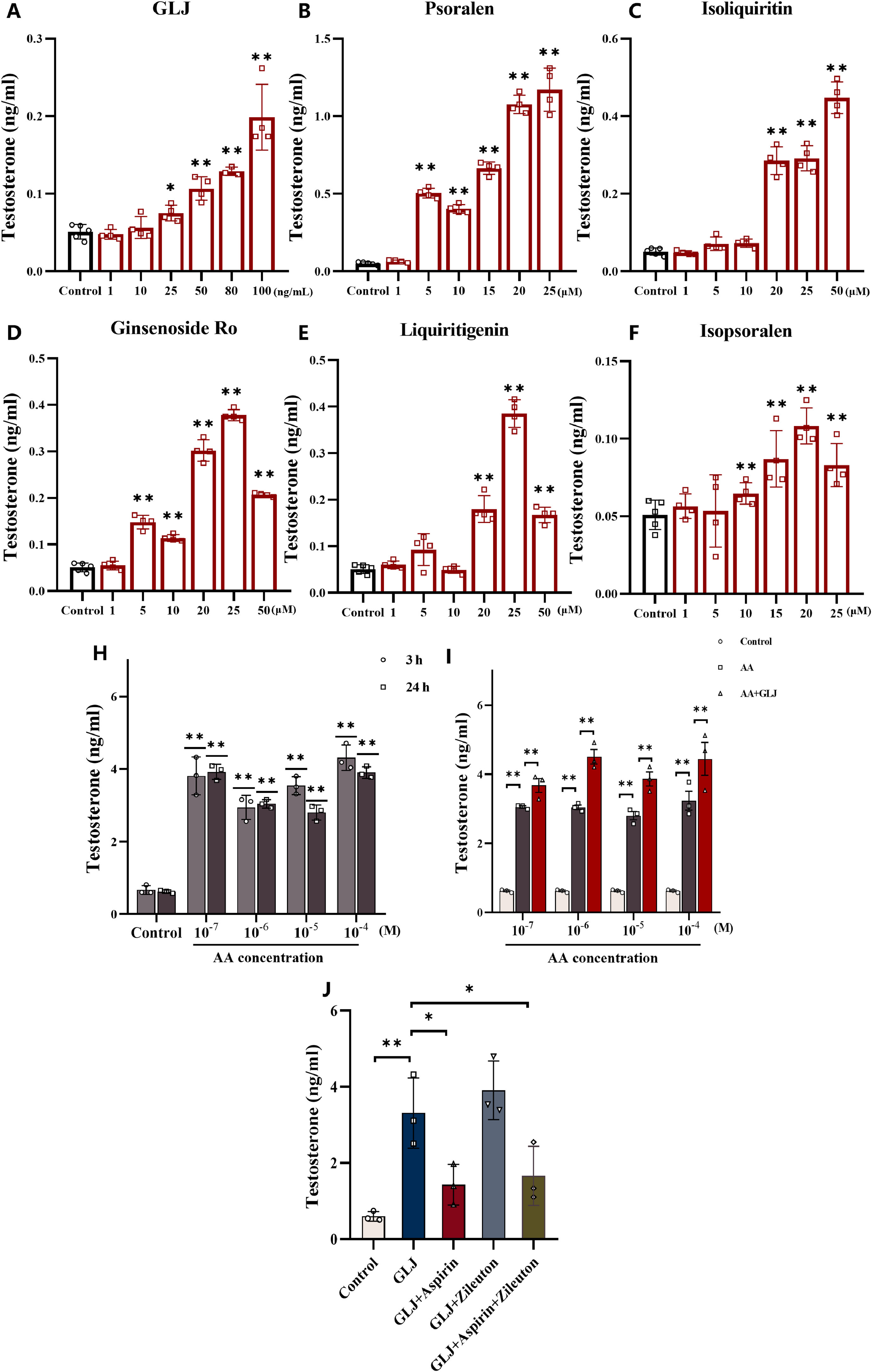
图7
7、花生四烯酸(AA)代谢参与睾酮分泌
如图7H-I所示,10-M-M的AA在处理3h和24h后极大地促进了TM3中睾酮分泌,但在处理3h和24h之间睾酮分泌没有显著差异。而且,GLJ(80ng/ml)可以促进AA的这种作用。图7J显示,单独使用GLJ(80ng/ml)可显著增加TM3的睾酮分泌,而阿司匹林(25μM,环氧化酶抑制剂)可显著降低GLJ的促进作用,抑制率为50%。与单独使用阿司匹林相比,联合使用阿司匹林和齐留通(25μM,脂氧合酶抑制剂)对GLJ的刺激具有相似的抑制作用。因此,加入阿司匹林后,GLJ对TM3分泌睾酮的促进作用明显受到抑制,而齐留通则没有。此外,给予AA、阿司匹林和齐鲁妥对TM3细胞的增殖没有有害影响。
总结:本文采用多组学+网络药理学方法,揭示GLJ对环磷酰胺诱导的OAT大鼠具有疗效,可调节脂质代谢和氨基酸代谢紊乱。花生四烯酸代谢可能是一个关键途径,而六个原型化合物是GLJ的潜在关键活性成分。傲星生物有丰富的分析方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




