《喜讯!Phytomedicine影响因子飙升至8.3分,这篇高价值模板,那叫一个真香!》
题目:甘草的抗结直肠癌作用及其通过HPLC整合和网络药理学方法的潜在机制
英文名:Anti-colorectal cancer actions of Glycyrrhiza uralensis Fisch. and its underlying mechanism via HPLC integration and network pharmacological approaches
杂志:Phytomedicine
影响因子:6.7
发表时间:2025年1月6日
研究背景:结直肠癌(CRC)发病率和死亡率高,现有治疗手段副作用显著。甘草在抗癌中具潜力,但其抗CRC的关键活性成分及机制尚不明确,亟需系统研究。
研究思路:本研究先通过HPLC鉴定甘草中的活性成分,再利用网络药理学筛选潜在靶点并构建“成分-靶点-通路”网络,结合分子对接和分子动力学模拟验证成分与靶点的结合能力,最后通过SW480细胞实验(增殖、迁移、侵袭等)和裸鼠异种移植模型实验,验证主要成分甘草苷(甘草苷)的抗CRC作用及机制。

研究结果:
1、甘草提取物中活性成分分析
基于前期实验和文献,对相关标准品和制备的甘草提取物进行HPLC分析。HPLC结果如图1A和B所示。通过样品与标准品的保留时间比较,检测到7种化合物:芦丁(图1C)、甘草查尔酮A(图1D)、甘草酸(图1E)、异甘草苷(图1F)、甘草素(图1G)、异甘草苷芹糖基(图1H)和甘草苷(图1I)。
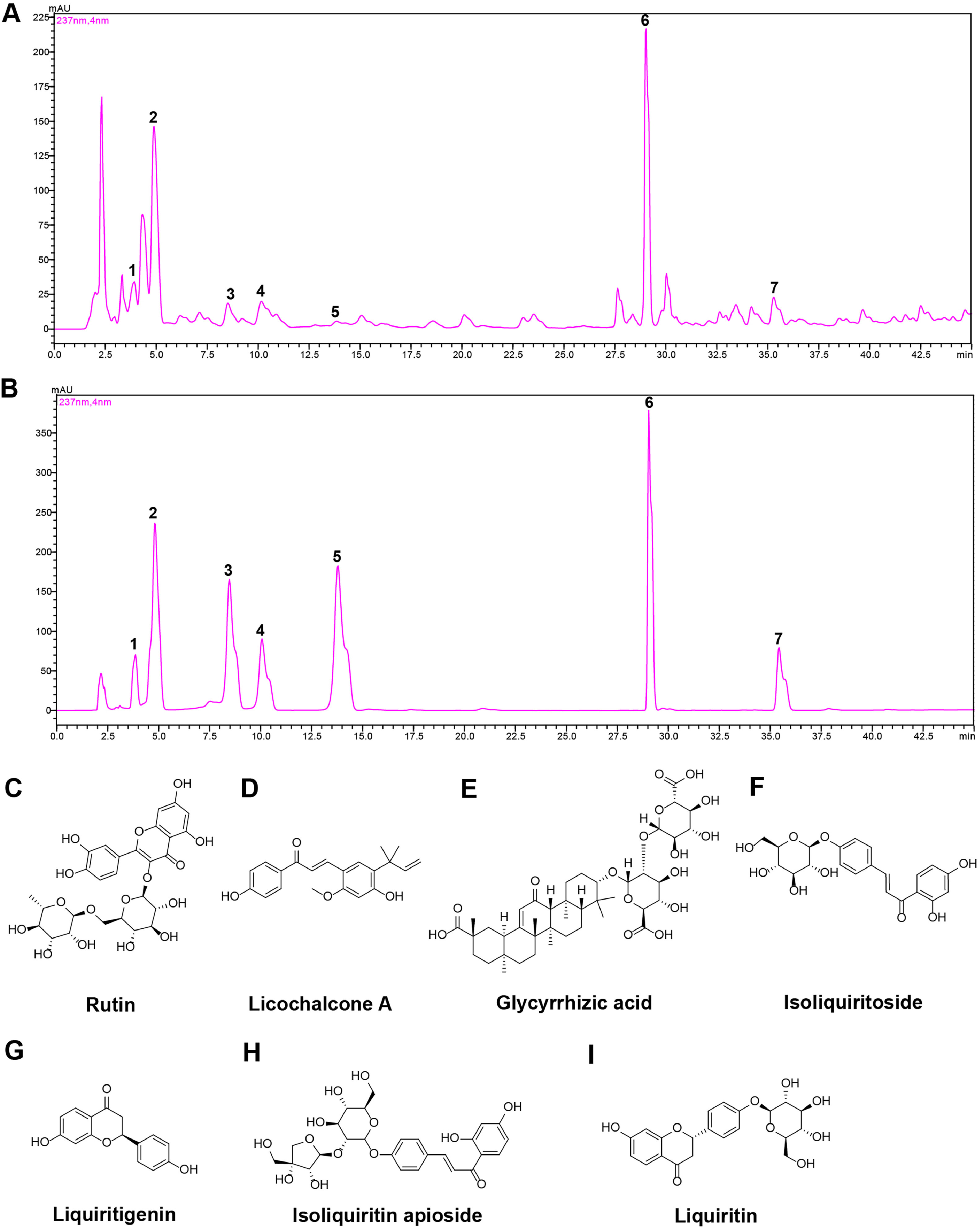
图1
2、甘草主要活性成分治疗CRC的网络药理学分析
从GeneCards数据库收集CRC(疾病)相关靶点,鉴定出322个与药物靶点相交的靶点(图2A)。如图2B所示,较大和较暗的节点表示可能与CRC关联更密切的靶点,鉴定出的靶点包括TP53、SRC、STAT3和PIK-3CA,成为前四个核心靶点,这些节点代表了甘草活性成分抗CRC的关键靶点,在其治疗效果中起核心作用。对七种活性成分治疗CRC的基因本体(GO)功能富集分析产生了1,285个GO术语(P<0.05),包括860个生物过程(BP)术语,涉及信号转导、蛋白质磷酸化、RNA聚合酶II启动子转录正调控、细胞凋亡负调控和细胞增殖正调控、炎症反应和蛋白质自磷酸化等(图2C)。在DAVID数据库中对七种活性成分与CRC的322个相交靶点进行分析,鉴定出177条KEGG通路,这些通路在CRC治疗的关键靶点中富集(图2D)。KEGG通路分析后,将通路中鉴定的靶点映射到其相应的化合物,并使用Cytoscape(3.7.2)构建“活性成分-靶点-通路”网络,结果显示该网络由279个节点和1,238条边组成,包括7个活性成分、252个靶点和20条信号通路(图2E)。这表明甘草的活性成分可以通过多种化合物和靶点作用于多个通路,共同促成治疗CRC的效果。
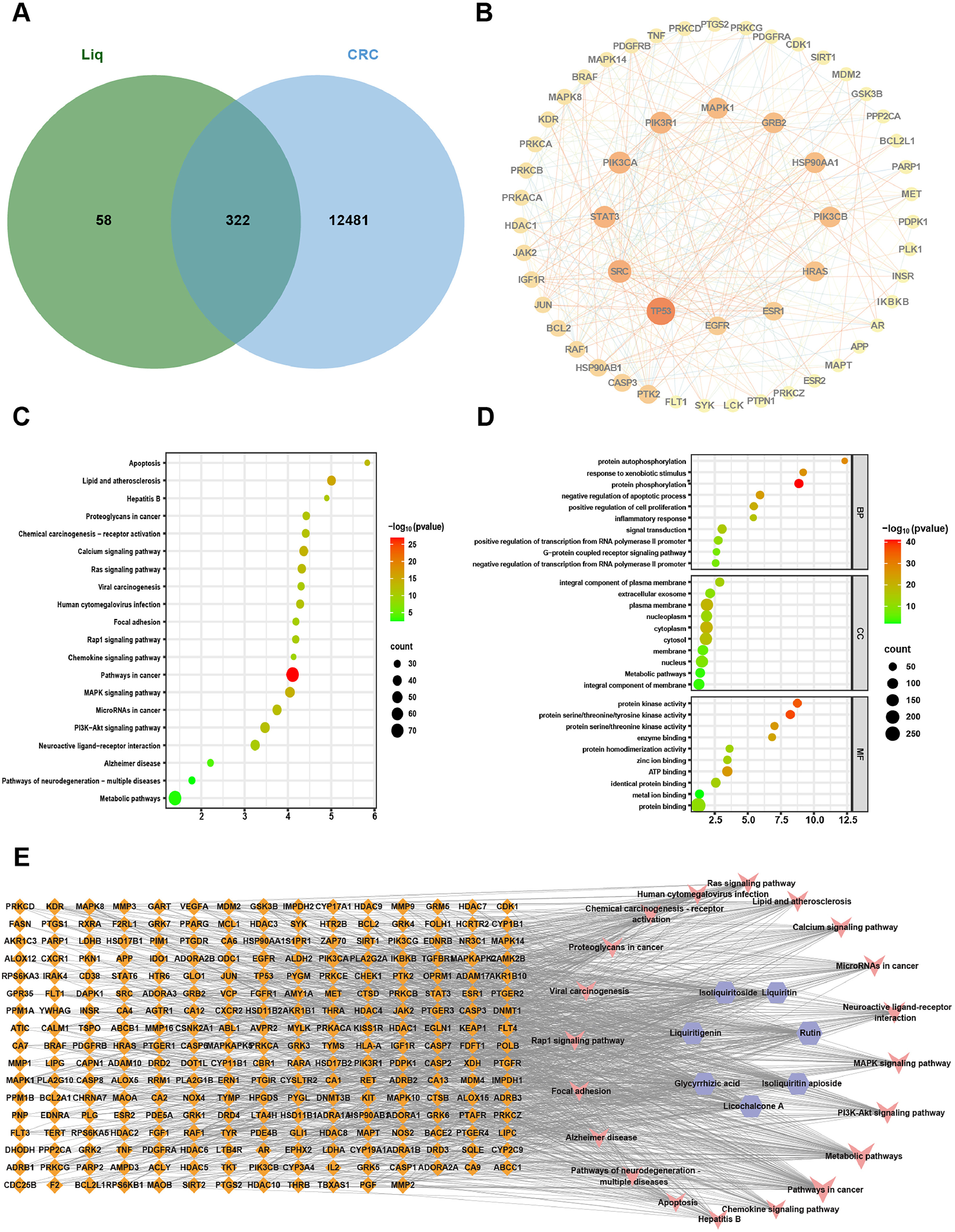
图2
3、分子对接和分子动力学模拟分析
对接能值<-4.25kcal/mol(1cal≈4.186J)通常是可接受的,表明分子之间有结合活性,而<-5.0kcal/mol和<-7.0kcal/mol分别表示良好和强结合活性。核心靶点基因与核心成分之间的结合能如图3B所示。在这些成分中,甘草酸表现出最强的结合能力,甘草苷排名第二。这两种活性成分与TP53、SRC、STAT3和PIK3CA蛋白的分子对接结果如图3A所示。如图3C所示,甘草苷-TP53复合体系在40ns后达到平衡,RMSD波动稳定在约2.2Å左右,表明配体与靶蛋白的结合稳定性高。进一步分析显示,模拟过程中回转半径(Rg)和溶剂可及表面积(SASA)的波动较小(图3D和E),表明配体结合后蛋白质的构象发生了变化。氢键在配体-蛋白质相互作用中起关键作用。如图3F所示,配体与蛋白质之间的氢键数量在0到4之间,平均约3个键,表明存在强氢键相互作用。均方根波动(RMSF)用于评估蛋白质中氨基酸残基的灵活性。如图3G所示,RMSF值相对较低(大多低于3Å),表明灵活性降低,稳定性增加。总之,甘草苷-TP53复合体系表现出高结合稳定性和强氢键相互作用,表明甘草苷与TP53的有效结合。
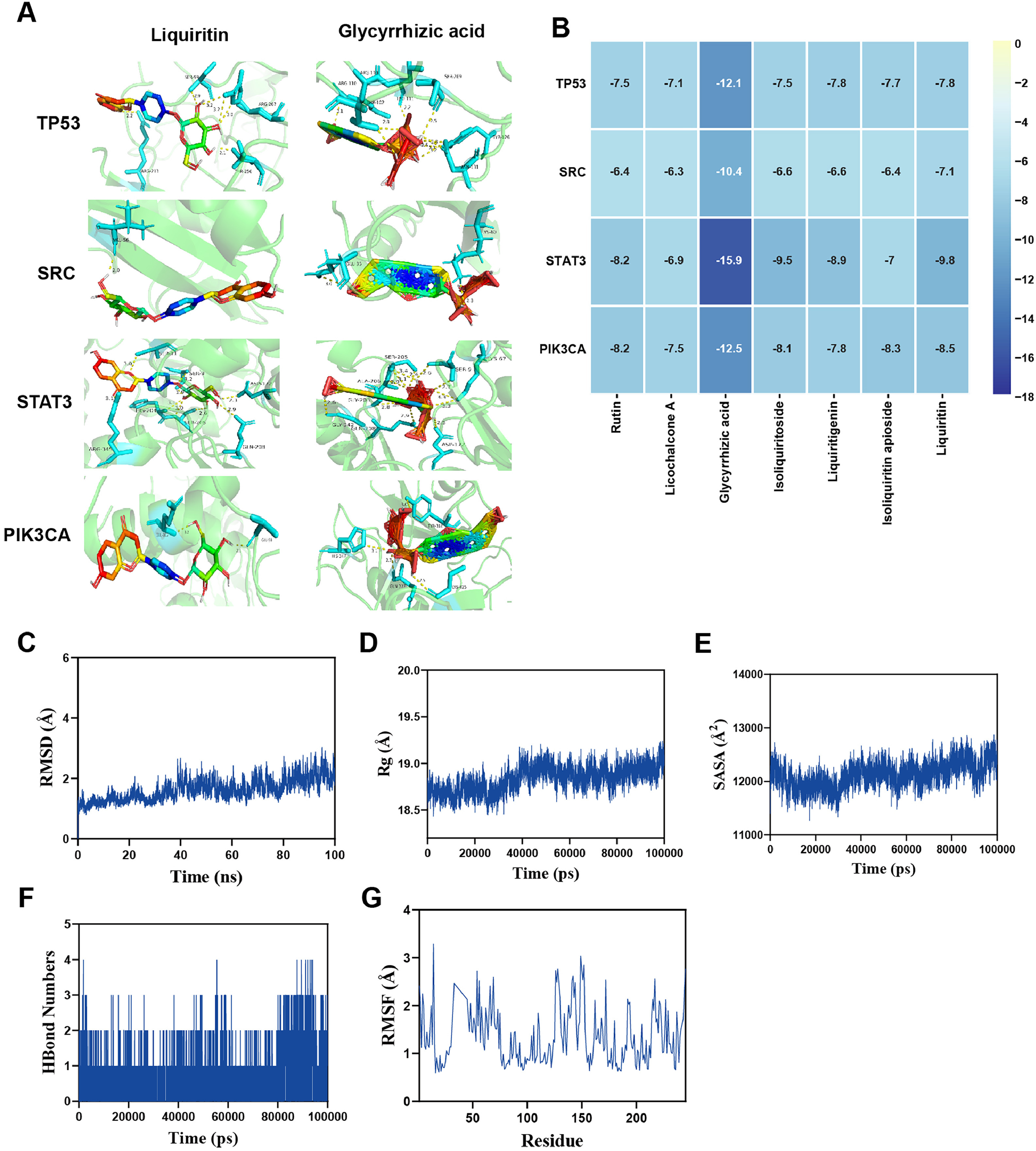
图3
4、体外实验
HPLC、网络药理学和分子对接数据结果表明,甘草中的甘草苷和甘草酸均对CRC表现出较强的抑制作用。因此,进行细胞实验以比较它们对CRC的抑制能力。如图4A和B所示,将不同浓度(μM)的甘草苷(25、50、100、200和400)应用于SW480细胞24和48小时,导致不同程度的细胞活力抑制,结果显示,甘草苷以剂量依赖性方式抑制SW480细胞的增殖,而甘草次酸则不然。因此,在后续实验中,选择50、100和200μM的甘草苷浓度进行48小时处理。集落形成实验的结果如图4C和D所示,与对照组相比,甘草苷组形成的细胞集落数量显著减少。同样,奥沙利铂组的细胞集落数量也减少,差异具有统计学意义(P<0.01)。用甘草苷(50、100、200μMol/L)处理SW480细胞48小时后,结果显示,与对照组相比,甘草苷以剂量依赖性方式促进SW480细胞凋亡,如图4E所示。
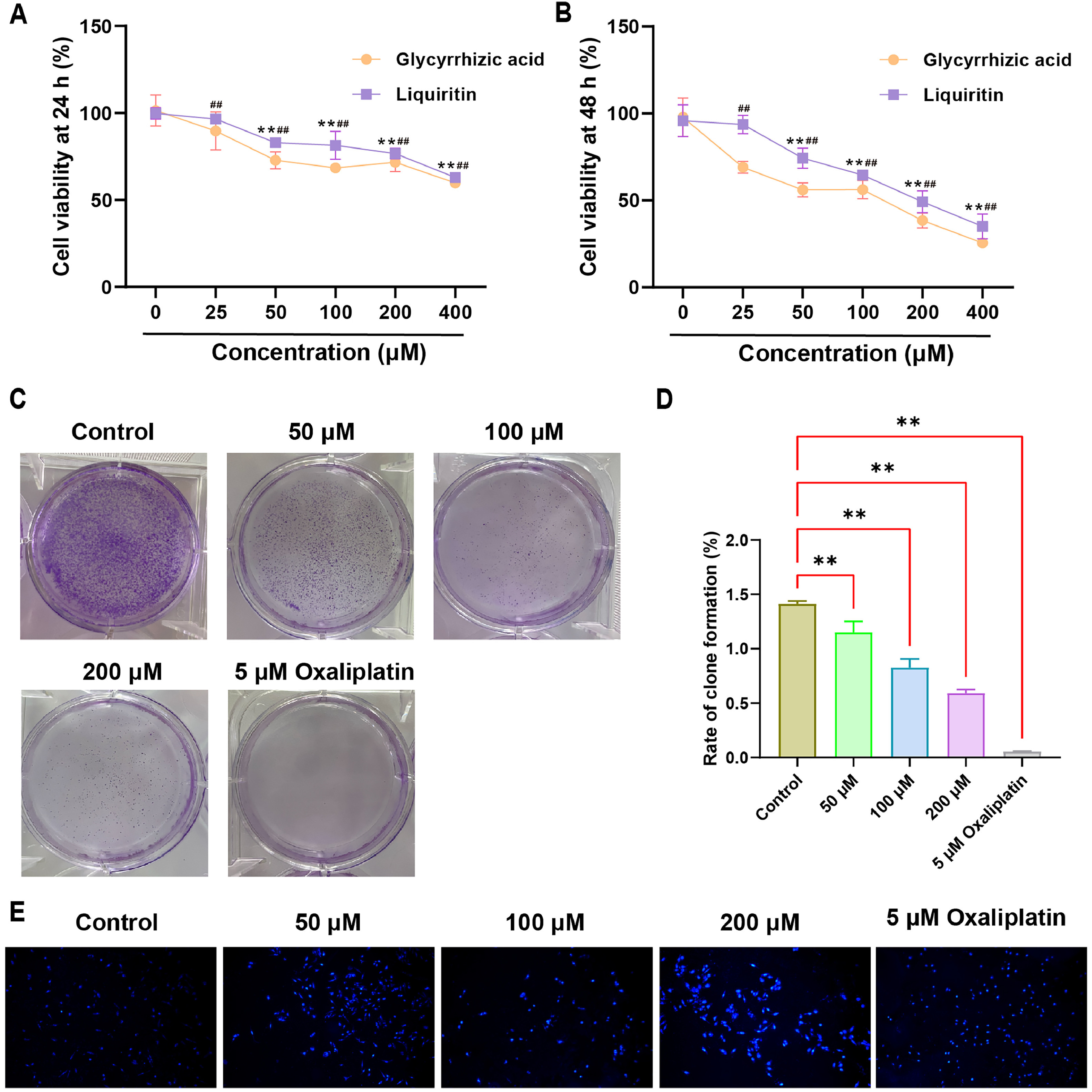
图4
5、甘草苷抑制SW480划痕、迁移和入侵实验
与对照组相比,阳性药物组的细胞迁移率和迁移细胞数量减少,如图5a和B所示,划痕区域愈合明显受到抑制,细胞迁移减慢。在药物处理组(48小时),50-200μM浓度显著抑制SW480细胞的迁移,表明甘草苷有效降低细胞的迁移能力,效果具有统计学意义(P<0.01)且呈浓度依赖性。使用Transwell方法评估甘草苷对SW480细胞迁移和侵袭能力的影响,如图5C-F所示,结果显示,处理48小时后,与对照组相比,阳性对照组的迁移细胞数量显著减少,差异具有统计学意义(P<0.01)。在200μM浓度的甘草苷组中,与对照组相比,细胞迁移和侵袭均减少,变化具有统计学意义(P<0.05),表明甘草苷有效减弱SW480细胞的迁移和侵袭能力。使用westernblot分析SW480细胞中侵袭蛋白的表达,结果显示,随着甘草苷浓度的增加,蛋白质水平显著下降。在200μM以及阳性对照组中,MMP蛋白(-1、-3和-9)的表达被显著抑制,此外,在100μM时,MMP-1的表达也显著降低(图5G-J),差异具有统计学意义(P<0.01)。研究结果表明,甘草苷可有效阻碍侵袭相关蛋白的表达,从而降低SW480细胞的侵袭潜力。
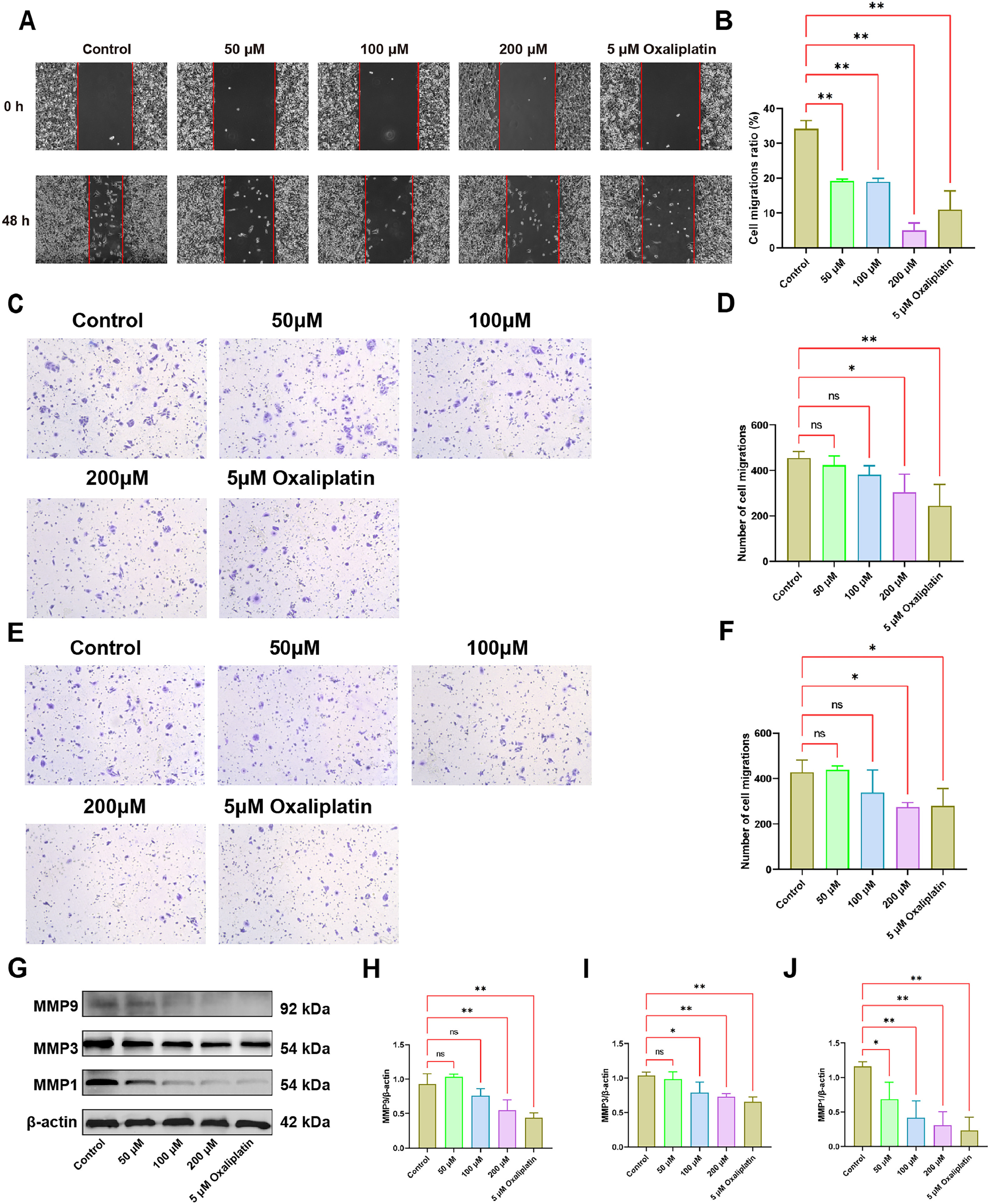
图5
6、甘草苷对裸鼠SW480异种移植模型状态和肿瘤大小的影响
在BALB/c裸鼠接种SW480细胞后的第3至4天,在右腋窝检测到可触及的实体瘤,然后在肿瘤植入后的第7天开始腹腔注射甘草苷,并持续12天。在实验过程中,模型组和治疗组的裸鼠均未死亡。肿瘤建模成功后,两组均表现出正常的饮食和活动,体重无明显变化。在治疗期间,甘草苷治疗组的整体状况优于模型组,各组之间体重无显著差异,且这些差异无统计学意义(图6A和B),表明甘草苷在体内给药是安全的。处死小鼠后,切除肿瘤并称重。如图6C和D所示,与模型组相比,甘草苷治疗组的肿瘤重量显著降低(P<0.05),且这种降低呈剂量依赖性,从而表明甘草苷对裸鼠SW480异种移植物的生长具有抑制作用。
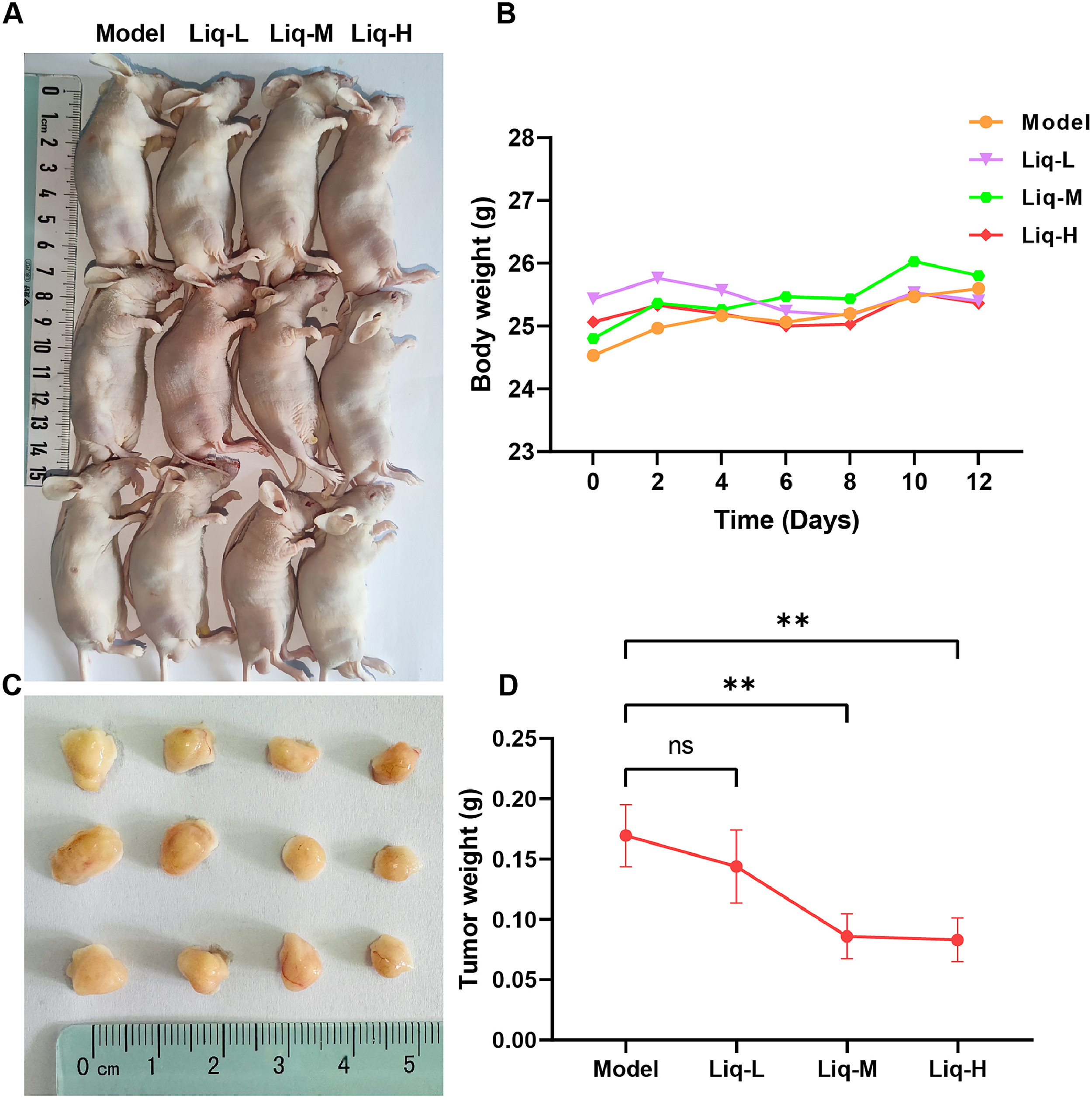
图6
7、甘草苷对裸鼠SW480异种移植肿瘤组织中p53/p38MAPK通路表达水平的影响
基于PPI网络、分子对接和KEGG通路分析,推测甘草苷可能通过靶向p53来调节MAPK信号传导,western blot结果显示,100和200μM甘草苷治疗组的p-p53/p53水平显著高于模型组(P<0.01),而任何浓度的p-p38MAPK/p38MAPK均显著降低(P<0.01)(如图7A和C所示)。HE染色结果证实,模型组的肿瘤组织表现出细胞弥漫性生长,细胞排列紧密,形态基本完整(如图7D所示)。这些发现表明,甘草苷导致裸鼠SW480异种移植组织发生显著的结构变化。因此,研究结果证实,甘草苷可能通过p53/p38MAPK信号轴抑制裸鼠SW480异种移植物的生长。
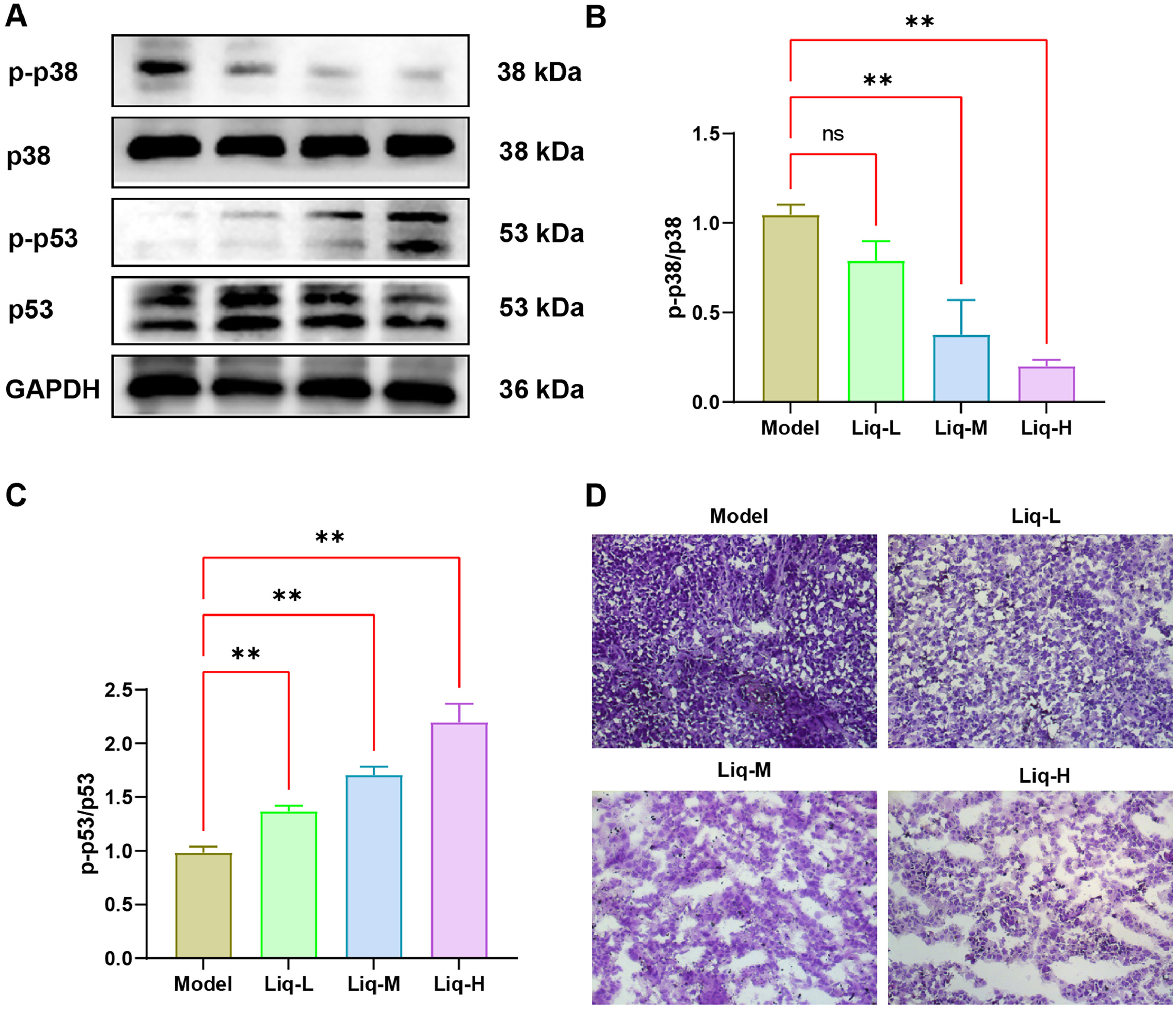
图7
总结:研究证实甘草中的甘草苷通过靶向p53并抑制p38MAPK通路,显著抑制CRC细胞增殖、迁移、侵袭及裸鼠肿瘤生长,为甘草治疗CRC提供了药理基础和潜在靶点。傲星生物深耕生信分析十余载,有丰富的实验方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




