IF=13.5!巧用自测+公共数据,低成本撬动高分成果!10+ Club 等你加入!
题目:三阴性乳腺癌异质性免疫微环境的多组学分析表明UQCRFS1增强肿瘤进展
英文名:Multi-omics analyses of the heterogenous immune microenvironment in triple-negative breast cancer implicate UQCRFS1 potentiates tumor progression
杂志:Exp Hematol Oncol
影响因子:13.5
发表时间:2025年6月16日
研究背景:三阴性乳腺癌(TNBC)通常以高级别和侵袭性特征为特征,导致患者远处转移的可能性增加,预后较差。肿瘤免疫微环境(TME)最近被认为与肿瘤进展和免疫治疗反应密切相关。然而,TNBC中实际的异质性TME仍有待探索。
研究思路:在自我测试的单细胞RNA测序数据集上对TME内的不同细胞类型进行全面分析,该数据集包含9例TNBC初治患者,包括亚簇分类、CellChat算法、转录因子(TFs)表达、伪时间分析和功能富集测定。通过拷贝数变异分析证实恶性上皮簇,随后进行LASSO-Cox回归,以5个关键基因为基础建立恶性细胞指数(MCI)模型,该模型通过Kaplan-Meier生存和免疫治疗反应分析在多个TNBC队列中得到验证。利用空间转录组、蛋白质组数据和qRT-PCR、western blotting实验来证实RNA和蛋白质水平的UQCRFS1表达。此外,还实施了功能实验以揭示UQCRFS1对TNBC细胞的影响。
 研究结果:
研究结果:
1、单细胞图谱涵盖TNBC患者的细胞组成
为解析未治疗三阴性乳腺癌的异质免疫微环境,收集9例患者的活检肿瘤组织进行单细胞RNA测序(图1A、B)。剔除低质量细胞后,最终获得92,304个细胞,将其分为8种主要细胞类型,即B细胞、内皮细胞、上皮细胞、成纤维细胞、壁细胞、髓系细胞、浆细胞和T细胞。基于患者标签或主要细胞类型的UMAP可视化如图2A、B所示,图2C显示了9例患者中8种主要细胞类型的比例。此外,这些主要细胞类型通过经典谱系标志物定义(图2D-F)。CellChat分析发现,成纤维细胞和髓系细胞在数量和强度上的相互作用最显著(图2G)。值得注意的是,成纤维细胞的输出信号频率highest,而髓系细胞的输入信号频率highest,表明它们在TNBC微环境中起重要作用(图2H)。总之,TNBC的异质TME基于多种细胞类型及其强烈的相互作用。
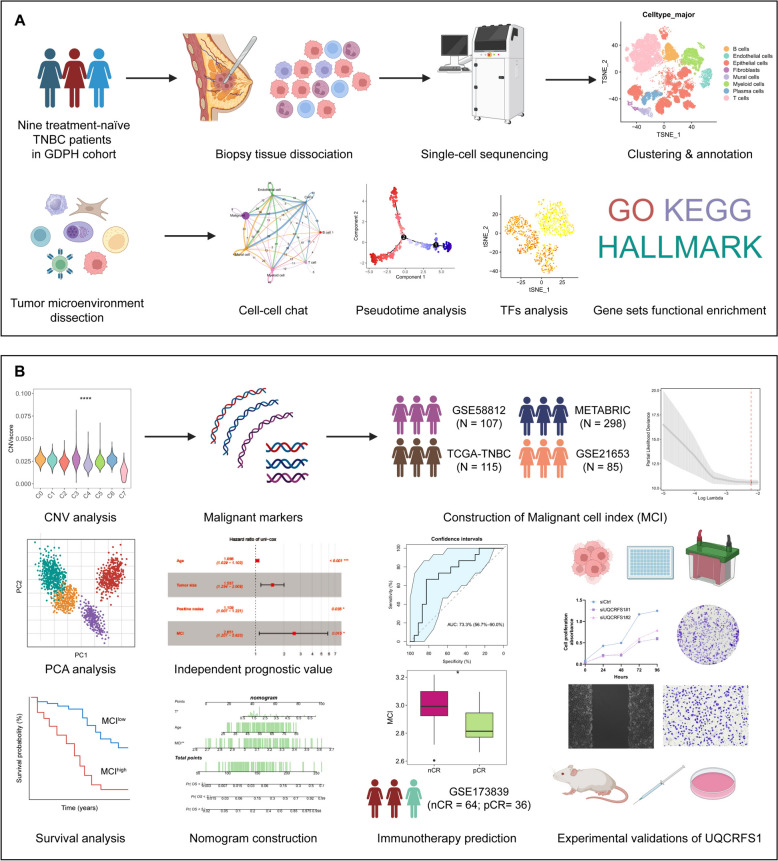
图1
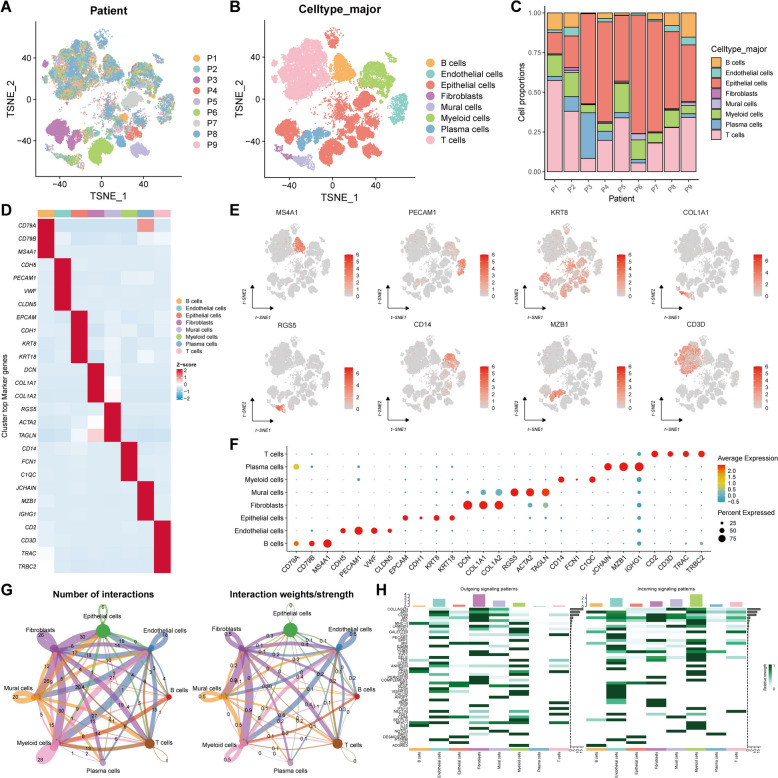
 图2
图2
2、三阴性乳腺癌中髓系细胞的特征
基于tSNE算法,髓系细胞被重新聚类为6个亚群,即巨噬细胞、肥大细胞、单核细胞、耐受性树突状细胞(tDCs)、浆细胞样DCs(pDCs)和常规DCs(cDCs)(图3A),亚群标志物如图3B、C所示。重点研究巨噬细胞,确认了4个亚群,包括S100A8+巨噬细胞、IL1B+巨噬细胞、FOLR2+巨噬细胞和MKI67+巨噬细胞(图3D)。小提琴图显示各亚群标志物的表达水平,证实聚类准确性(图3E)。此外,CellChat分析发现巨噬细胞各亚群间存在广泛通讯(图3F)。功能富集分析显示各亚群富集不同通路(图3G)。代谢分析表明FOLR2+和MKI67+巨噬细胞代谢活性较高(图3H)。转录因子分析发现各亚群转录因子表达不同,且与不良预后相关(图3I、J)。总之,髓系细胞尤其是巨噬细胞的异质性与TNBC不良预后相关。
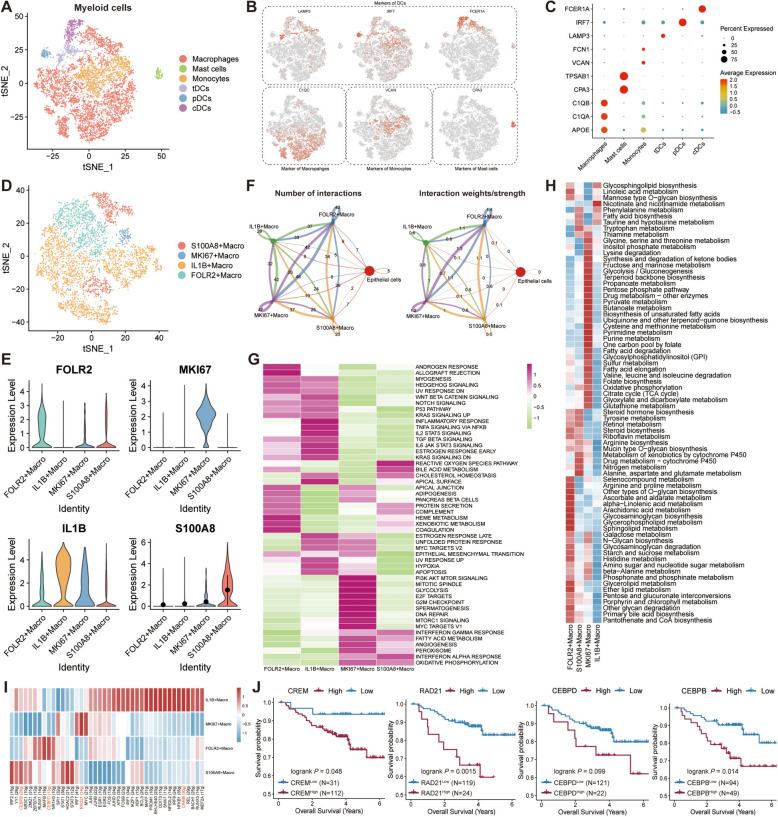
 图3
图3
3、三阴性乳腺癌中成纤维细胞和B/浆细胞的多样性
越来越多的证据表明,原发或转移性肿瘤的成纤维细胞具有显著的适应性、可塑性和韧性,通过与TME中的各种细胞群相互作用促进肿瘤进展[44]。对成纤维细胞进行重新聚类,基于tSNE算法明确了4个集群(Fib_C0-C3)(图4A)。热图显示这些集群间的差异表达基因(图4B)。CellChat分析表明Fib_C0和Fib_C1集群的通讯比Fib_C2和Fib_C3更频繁(图4C)。拟时序分析显示从Fib_C2到其他集群的分化轨迹(图4D、E)。KEGG富集分析发现Fib_C0和Fib_C1富集多种通路(图4F)。表面蛋白基因表达比较显示Fib_C0和Fib_C1与多种extracellular基质等相关基因相关(图4G)。随后,确认了2个B细胞亚群(naive和记忆B细胞)和2个浆细胞亚群(JCHAIN+和IGG+浆细胞)(图4H),各亚群标志物如图4I、J所示。Monocle分析阐明了从B细胞到浆细胞的分化过程(图4K)。通路富集分析显示naive和记忆B细胞免疫调节通路活跃,而浆细胞亚群泛素介导的蛋白水解等通路活跃(图4L)。转录因子分析显示浆细胞亚群XBP1表达升高,B细胞亚群STAT1表达升高(图4M、N)。总之,成纤维细胞和B细胞的多样性在分化轨迹等方面得到阐明。
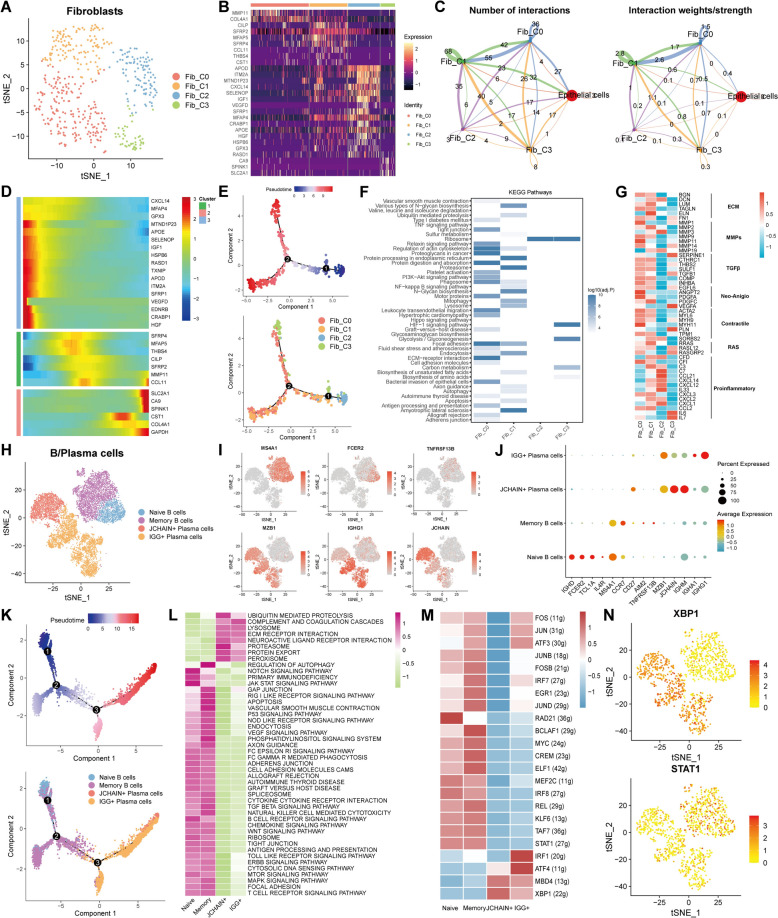
 图4
图4
4、三阴性乳腺癌中T/NK细胞的区分
T细胞和NK细胞也是TME的重要组成部分。筛选出T/NK细胞并重新命名,鉴定出CD4+T细胞、CD8+T细胞、调节性T细胞(Tregs)、MKI67+T细胞、NK细胞和NKT细胞(图5a),各细胞类型标志物如图5B所示。CD4+T细胞、CD8+T细胞和Tregs的亚群如图5C、D所示。CellChat分析发现各亚型与上皮细胞的通讯存在差异(图5E)。免疫相关基因表达和功能评分显示各亚型存在显著差异,IL32high Treg在免疫逃逸中起重要作用(图5F、G)。通路富集分析显示IL32high Treg富集更多免疫失调相关通路(图5H)。生存分析表明IL32high Treg浸润多的患者预后差(图5I)。总之,TNBC免疫细胞异质性显著,IL32high Treg可能促进免疫逃逸。
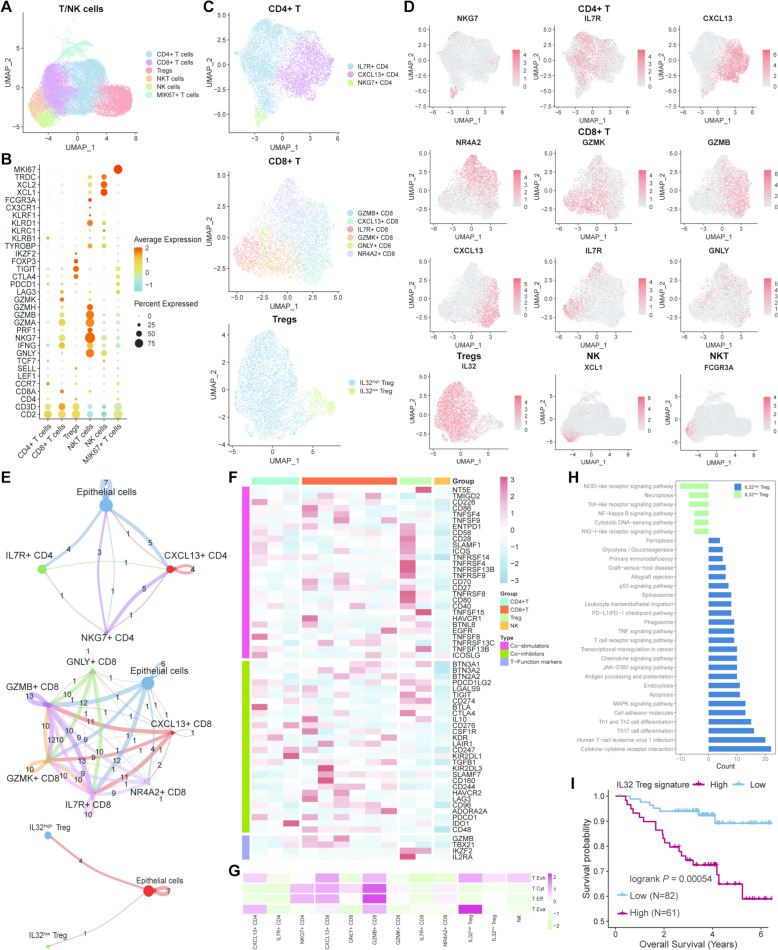
 图5
图5
5、三阴性乳腺癌上皮细胞集群亚群的区分
为确定TNBC上皮细胞的异质性,通过“inferCNV”算法识别正常和恶性上皮细胞,并对恶性细胞进行重新聚类,确定8个亚群(Malignant_C0–C7)(图6A、B)。各集群标志物如图6C所示。CNV评分比较显示Malignant_C3的CNV评分显著高于其他集群(图6D)。CellChat分析显示Malignant_C5的互作数量最多(图6E)。功能富集分析显示各亚群参与不同功能通路(图6F、G)。转录因子和免疫相关基因表达分析显示各亚群存在差异(图6H、I)。总之,TNBC恶性细胞亚群的独特特征可能通过多种功能通路对TME发展起重要作用。

图6
6、基于三阴性乳腺癌恶性上皮标志物的MCI构建和验证
为挖掘恶性上皮细胞中差异表达标志物的临床价值,利用单变量Cox回归和LASSO算法在TNBC患者的bulk转录组数据中筛选出具有预后意义的恶性基因。训练集包括GSE58812和TCGA-TNBC数据集,验证集包括METABRIC和GSE21653数据集。通过单变量Cox回归和重叠分析,在训练集中筛选出28个共同基因(图7A、B),最终通过LASSO算法选择5个基因构建恶性细胞指数(MCI)(图7C)。PCA分析显示在训练和验证队列中基于MCI的区分效果良好(图7D)。MCI值调整后显示MCIhigh组死亡患者比例可能更高(图7E)。热图显示5个关键基因在MCIhigh患者中均上调(图7F)。Kaplan-Meier生存分析显示MCIhigh患者生存率显著降低(图7G)。总之,内部训练和外部验证表明MCI在监测TNBC患者生存结局方面具有潜力。
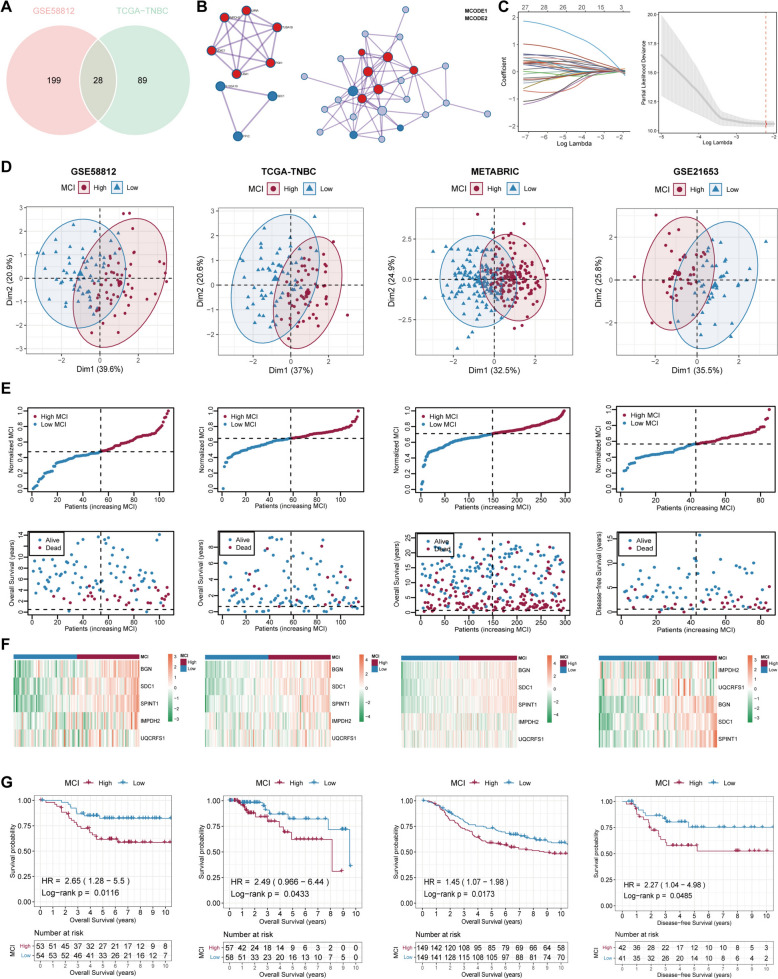
 图7
图7
7、MCI能够预测三阴性乳腺癌患者的免疫治疗反应
森林图显示在GSE58812队列中,MCI是独立预后指标(图8A、B)。通过多变量Cox和逐步回归分析构建列线图模型,可估计2、3和5年OS概率(图8C)。校准曲线显示预测与观察的生存率一致性良好(图8D)。决策曲线分析显示列线图性能优于其他预测因子(图8E)。列线图评分分析显示低评分患者预后更好(图8F)。为探索MCI是否与免疫治疗反应预测相关,收集接受ICB(度伐利尤单抗联合奥拉帕利)和紫杉醇治疗的TNBC患者的转录组数据。计算每位患者的MCI,结果显示对ICB无病理完全缓解(nCR)的TNBC患者MCI值高于有病理完全缓解(pCR)的患者(图8G)。基于MCI中位数分组,MCIhigh亚组nCR患者比例显著更高(图8H)。ROC分析显示AUC值为0.733(图8I)。此外,在7例接受新辅助ICB治疗的患者中验证,nCR组累积MCI更高(图8J-M)。各主要细胞类型中,除正常上皮细胞外,nCR组MCI值显著升高(图8N)。总之,这些发现表明MCI可预测TNBC患者的免疫治疗不良反应。
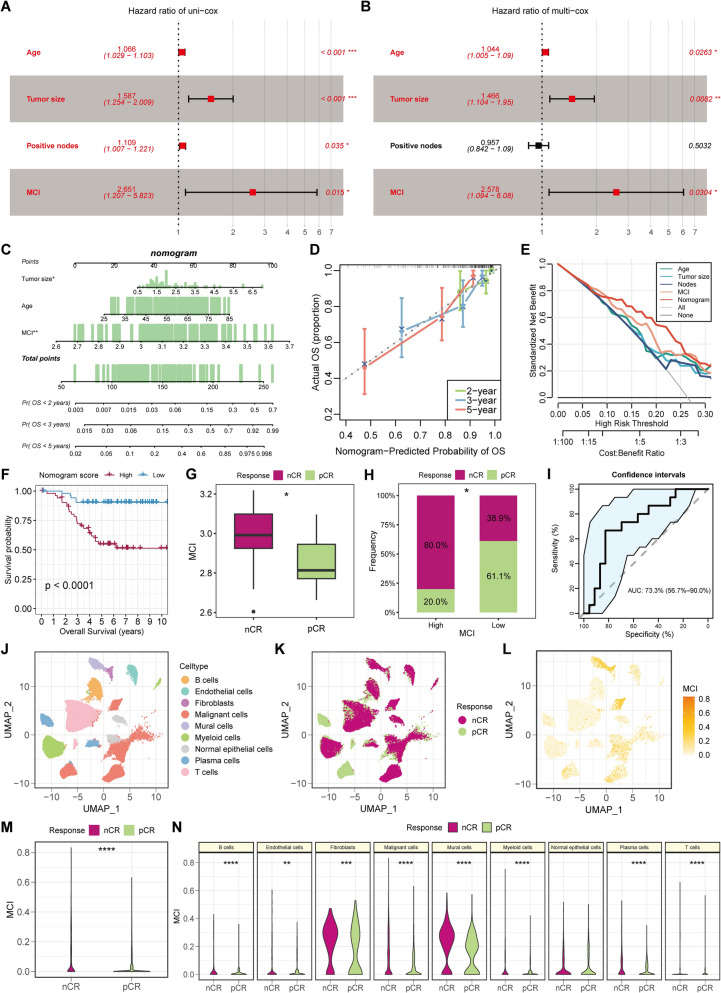
 图8
图8
8、UQCRFS1是潜在生物标志物,促进TNBC细胞的增殖和迁移
为探索UQCRFS1在TNBC中的表达和临床意义,在GSE76250数据集中比较配对的非肿瘤和TNBC样本中UQCRFS1的表达,显示TNBC组织中UQCRFS1明显升高(图9A)。qRT-PCR发现TNBC细胞系中表达高于乳腺上皮细胞系MCF-10A(图9B)。FUSCC蛋白质组数据显示UQCRFS1蛋白在TNBC组织中上调(图9C)。Westernblot分析证实TNBC细胞系中UQCRFS1蛋白水平显著升高(图9D)。收集含1例TNBC患者的空间转录组数据集,显示UQCRFS1主要在肿瘤区域表达(图9E、F)。
此外,为探究UQCRFS1对TNBC细胞的功能影响,在MDA-MB-231和BT549细胞中敲低UQCRFS1(图9G),进行一系列体外和体内功能实验。CCK-8实验显示敲低UQCRFS1显著抑制TNBC细胞增殖(图9H)。Transwell和集落形成实验显示敲低UQCRFS1显著抑制迁移和集落形成(图9I-K)。体内实验中,稳定敲低UQCRFS1的MDA-MB-231和BT549细胞构建异种移植模型(图9L),发现敲低UQCRFS1可抑制异种移植肿瘤的重量和生长曲线(图9M-P)。总之,这些结果表明UQCRFS1在体外和体内促进TNBC细胞增殖和迁移,提示其可能是TNBC的潜在生物标志物。
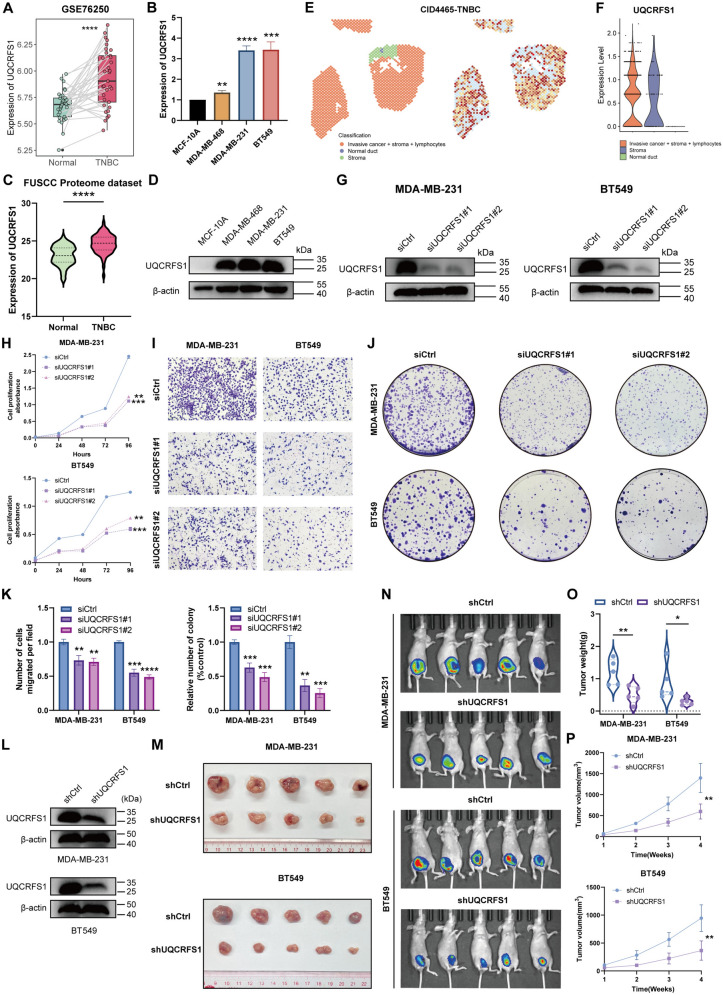
图9
总结:研究揭示TNBC免疫微环境异质性,发现IL32high Treg与不良预后相关,构建的MCI模型可预测预后及免疫治疗耐药,UQCRFS1可促进TNBC进展,为治疗提供新靶点。傲星生物深耕生信分析十余载,有丰富的实验方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




