IF:8.3,多组学+孟德尔随机化+网络药理学,揭秘广藿香醇重塑肠道菌群-神经轴,缓解肠易激综合征机制!
题目:广藿香醇通过肌球蛋白Va介导的神经递质调控恢复腹泻型肠易激综合征肠道稳态
英文名:Patchouli alcohol restores gut homeostasis in irritable bowel syndrome with diarrhea through myosin Va-mediated neurotransmitter regulation
杂志:Phytomedicine
影响因子:8.3
发表时间:2025-03-20
研究背景:腹泻型肠易激综合征(IBS-D)全球成人患病率约4–10%,以腹痛、腹泻、内脏高敏为特征,目前病因未明、治疗靶点缺乏。肠神经系统(ENS)兴奋-抑制神经元失衡导致胃肠动力异常,而肌球蛋白Va(MYO5a)在神经递质囊泡运输中起关键作用。广藿香醇(PA)是经典药食同源中药广藿香的活性成分,临床可缓解IBS-D症状,但其作用机制尚不清楚。
研究思路:本研究首先整合GEO、UKB、GTEx公共数据库,通过差异基因分析、孟德尔随机化和网络药理学锁定ENS神经递质及MYO5a为PA潜在靶点;随后建立慢性束缚应激IBS-D大鼠模型及MYO5a缺陷DBA小鼠模型,采用16SrRNA、全转录组、snRNA-seq多组学联合离体肌张力、免疫荧光、qPCR、WB、基因敲低/过表达等功能实验,系统验证PA通过上调MYO5a恢复ENS神经元亚型稳态、重塑结肠纵行肌间神经丛(LMMP)神经递质释放,从而改善IBS-D胃肠动力和微生态失衡。
研究结果:
1、转录组分析揭示IBS-D人群差异表达基因
转录组数据集(GSE146853)分析出396个差异表达基因,其中HTR3C/HTR3E、CHAT、TAC1和SLC18A3上调,而MYO5a、一氧化氮合酶(NOS)1、VIP、INHBC和CHRM2下调(图2A-C)。GO通路富集分析表明,上调基因与5-羟色胺受体信号通路调节、兴奋性突触后电位调节等,而下调基因与调节平衡和免疫调节的神经肌肉过程相关,包括G蛋白偶联神经递质受体活性、DNA修复和TGF-β受体结合(图2D-F)。此外,KEGG通路富集分析显示上调基因参与胆碱能突触、神经活性配体-受体相互作用、氧化应激反应等过程相关(图2G-I)。
2、基因eQTL孟德尔随机化明确基因与疾病关联
为进一步阐明上述基因与IBS-D的相关性,进行了基因eQTL孟德尔随机化分析(图2O)。各种MR方法对这些基因的方向与IVW方法一致,表明这些方法揭示的因果效应是一致的(图2J-N)。结果表明这些基因的变异与疾病发病存在因果关系,敏感性分析证实结果稳健可靠。
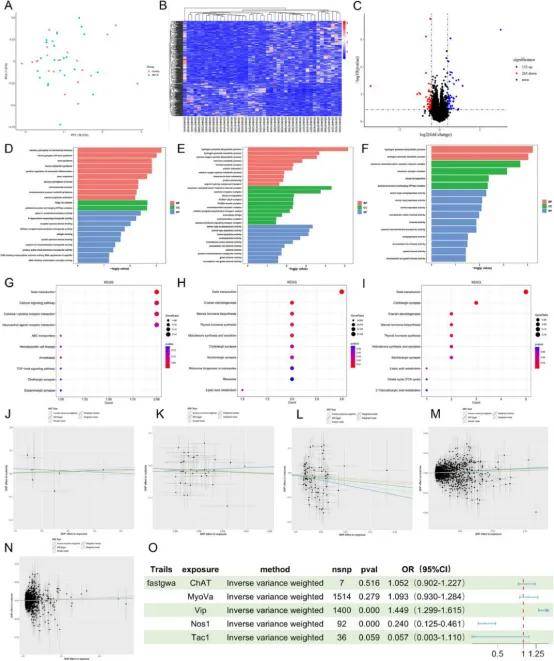
图2
3、网络药理学和分子对接验证药物靶点
网络药理学分析获得PA与IBS-D的40个交集靶点(图3A)。PPI网络显示7个与ENS和胃肠道消化系统密切相关的靶基因(图3B)。GO分析表明这些基因富集于细胞钙离子稳态等与肠神经元活性密切相关的活动(图3C-E)。KEGG通路富集显示这些靶基因在消化系统疾病通路中富集(图3F-G)。分子对接预测PA与12个潜在核心靶蛋白有较强结合亲和力(图3H-S),表明PA可能通过调节与ENS密切相关的蛋白质影响肠神经递质释放。
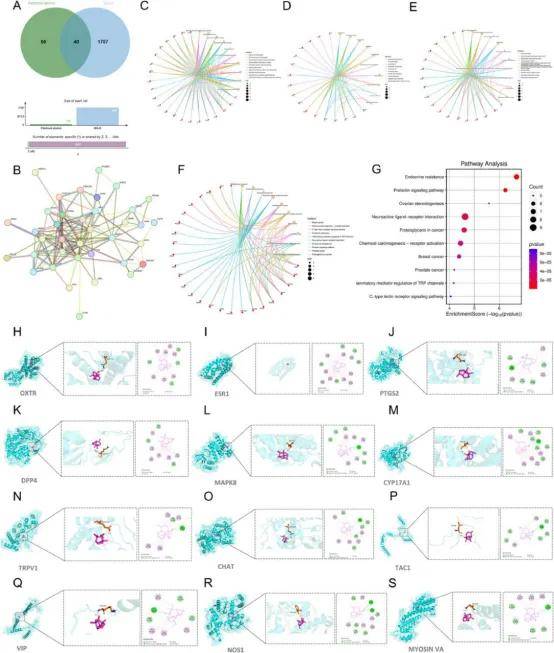
图3
4、PA改善IBS-D模型大鼠胃肠道相关症状
慢性束缚应激诱导的IBS-D大鼠模型显示,与对照组相比,模型组在第14、21和28天的粪便面积、粪便颗粒数(图4D,G,J)、AWR评分(图4A-C,F)、总胃肠道传输率(图4H)和粪便含水量(图4I)显著增加。结肠珠排出时间在第14和28天显著缩短(图4K),表明IBS-D大鼠表现出明显腹泻、肠道运动亢进和内脏高敏感性。PA给药显著缓解这些症状。离体实验显示IBS-D大鼠结肠肌条自主收缩(图4L-P)和8-32Hz电场刺激下的肌张力(图4Q-U)显著升高,PA给药呈剂量依赖性显著降低收缩张力,EC50为41.9μmol/l。各组结肠组织未见明显病理变化(图4V)。
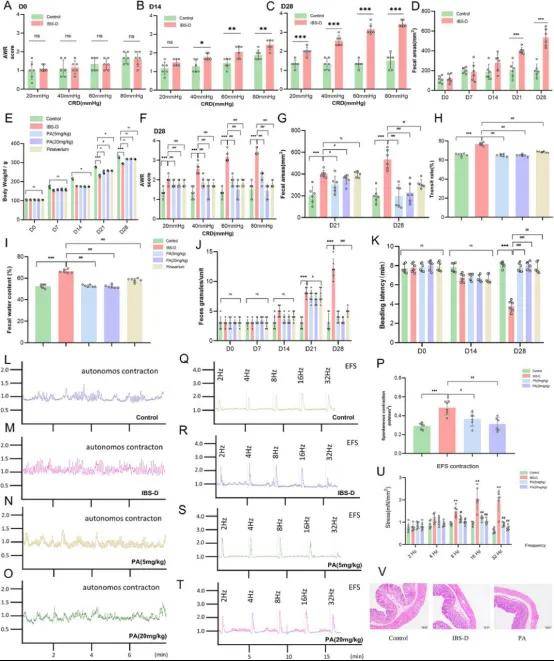
图4
16SrRNA测序显示三组大鼠肠道菌群多样性变化显著(图5a,B)。Chao1和Shannon指数表明IBS-D组的肠道菌群紊乱与正常组明显不同(图5C,D)。IBS-D组中厚壁菌门与拟杆菌门的比例以及变形菌门和脱硫杆菌门的丰度增加(图5E)。同时,有害菌群如Escherichia-Shigella和NK4A214.group升高,而有益菌群如Bacteroides和Lactobacillus减少(图5F)。PA治疗后,肠道菌群组成改善,有害菌减少,乳酸菌等益生菌丰度恢复(图5G-J)。
免疫荧光显示,与对照组相比,第28天模型组远端结肠LMMP神经元总数显著增加,PA给药恢复神经元数量(图5K,L)。这些结果表明慢性束缚应激成功建立了IBS-D大鼠模型,PA给药显著减轻症状,其作用机制与ENS密切相关。
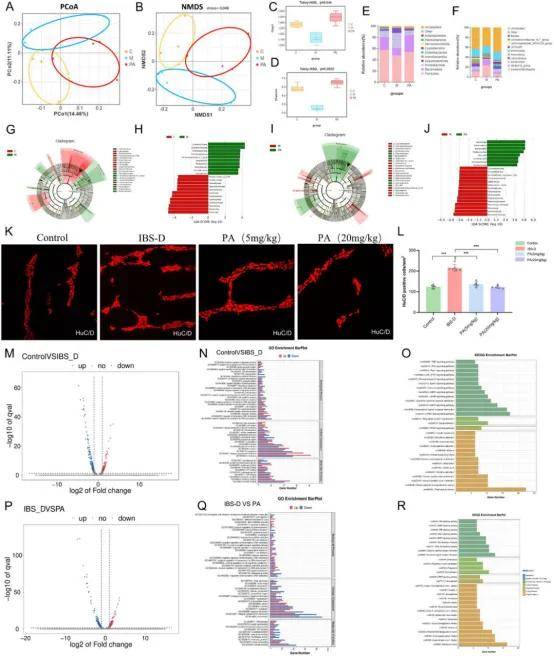
图5
5、PA改善IBS-D大鼠神经稳态失衡
LMMP参考转录组测序和snRNA-seq结果显示,与对照组相比,IBS-D组240个基因上调和213个基因下调(图5M)。GO和KEGG富集分析强调影响ENS神经元活性的生物过程,包括apelin、钙和cAMP信号通路(图5N,O)。与IBS-D组相比,PA组174个基因上调和240个基因下调(图5P)。GO富集结果显示基因通路显著富集于与肠神经活性密切相关的生物过程。KEGG通路富集于PI3K-Akt信号通路等与ENS发育和神经可塑性密切相关的通路(图5Q,R)。
单细胞测序鉴定了11种细胞类型(图6A),对照组相比,IBS-D组成熟肠神经元(HuC/D+)总数和比例显著增加(1142vs.2244;4.6%vs.8%)(图6B),神经元细胞中前20个基因的GO通路主要富集于胆碱能突触等信号通路(图6C)。KEGG通路主要富集于神经退行性疾病以及消化系统疾病(图6D)。分组GSEA和GSVA表明IBS-D组的基因集主要富集于糖皮质激素生物合成、炎症性肠病和平滑肌正向调节等过程(图H)。
PA给药降低了IBS-D大鼠远端结肠肠神经元总数,同时下调兴奋性神经元(ChAT+和SP+)的数量和比例(图K),表明PA可能通过改变结肠LMMP神经元及其亚型的数量和功能来增强胃肠动力和减轻大鼠高敏感性,恢复肠神经稳态。
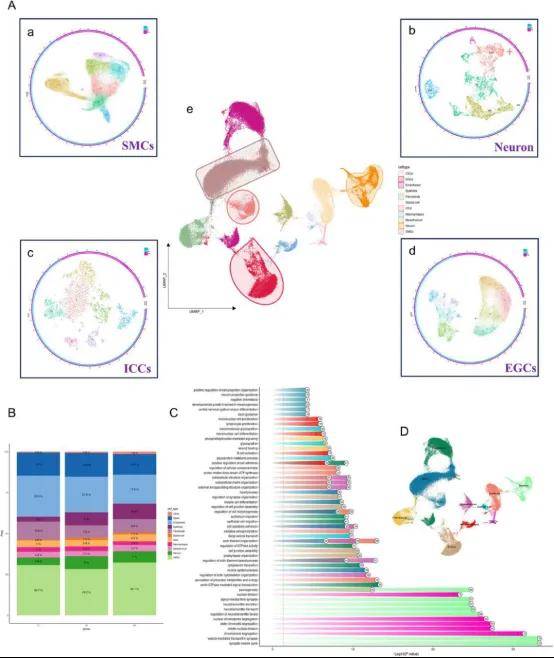
图6
6、PA对IBS-DLMMP抑制性神经递质相关基因和蛋白的影响
免疫荧光显示,与对照组相比,模型组远端结肠LMMP nNOS-和VIP阳性神经元的数量和比例显著减少,各PA剂量组显著上调并恢复正常水平(图7A-C,G,I,J)。qPCR显示远端结肠LMMP、nNOS和VIP的mRNA表达显著下调,PA给药后各治疗组基因表达显著上调(图7D,K)。WB显示远端结肠LMMP、nNOS和VIP蛋白表达水平下调并显著低于对照组,PA给药后各治疗组蛋白表达呈上升趋势(图7E,F,H,L)。

图7
分离培养大鼠结肠LMMP条带获得细胞悬浮液,观察神经元生长(图8A)。神经元显示典型形态特征,免疫荧光鉴定(图8B)。与静息状态相比,90mMK+溶液条件下结肠神经元NO释放增加,L-NAME应用后减少(图8C,E)。IBS-D大鼠结肠神经元NO释放水平无明显变化,而PA预孵育增强肠神经元NO释放,且不被L-NAME抑制(图8G,I)。但当nNOS被L-NAME抑制后再治疗,仅高剂量PA(20μmol/l)促进NO释放(图8H,J)。

图8
7、PA对IBS-DLMMP兴奋性神经递质相关基因和蛋白的影响
免疫荧光显示,与对照组相比,IBS-D模型组大鼠远端结肠LMMP SP-和ChAT阳性神经元的数量和比例显著升高,各PA剂量组显著降低并恢复正常水平(图9A-C,G,I,J)。qPCR显示模型组LMMP、SP和ChAT mRNA表达显著增加,PA给药后各治疗组mRNA表达显著下调(图9D,K)。WB显示SP和ChAT蛋白表达水平上调并显著高于对照组,PA给药后蛋白表达呈下降趋势(图9E,F,H,L)。snRNA-seq显示与对照组相比,IBS-D模型动物LMMP神经元总数(1142vs.2444)和比例(4.6%vs.8%)显著增加(图6B)。神经元与SMCs的比例增加86.7%,但PA治疗2周后该比例降低21.4%,接近正常水平。
PA拮抗CCh诱导的平滑肌收缩,使CCh的EC50增加约40倍。当用L-NAME(10μmol/l)抑制氮能通路时,IBS-D模型大鼠结肠平滑肌出现收缩,但PA预孵育有效抑制这种效应,表明PA通过多种神经通路抑制结肠平滑肌收缩。
体内外实验结果表明,IBS-D大鼠ENS稳态被破坏,结肠平滑肌收缩频率和幅度增加,兴奋性和抑制性神经元失衡。PA给药可改善大鼠胃肠动力障碍和内脏高敏感性,有效调节兴奋性和抑制性神经元平衡,恢复肠神经稳态。
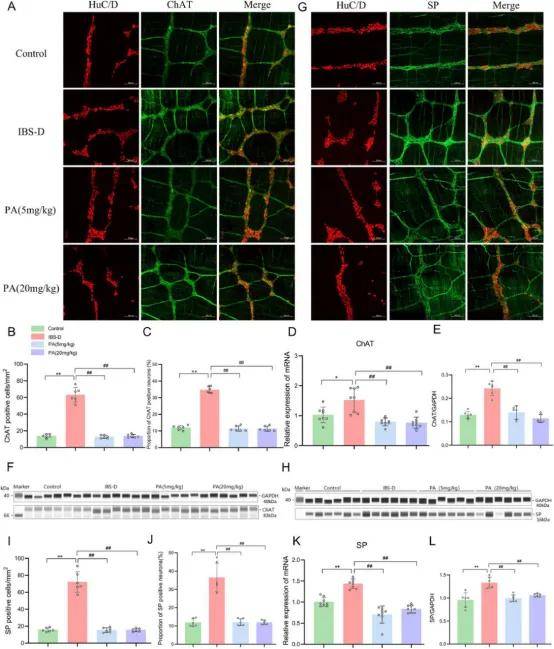
图9
8、PA通过精确调控肌球蛋白Va调节神经递质传导治疗IBS-D
免疫荧光显,PA给药2周后,低剂量和高剂量PA组大鼠远端结肠LMMPmyosin Va荧光强度增加,myosin Va mRNA和蛋白相对表达水平增加(图10A-E)。
免疫荧光研究了myosin Va在结肠神经元内与抑制性和兴奋性神经递质相关蛋白nNOS、VIP、ChAT和SP的共定位。结果显示显著共定位。共定位系数分析显示,与对照组相比,模型组远端结肠LMMP myosin Va与nNOS、VIP、ChAT和SP的Pearson相关系数和Mander重叠系数降低,低剂量和高剂量PA给药后这些系数高于模型组(图10F-Q)。
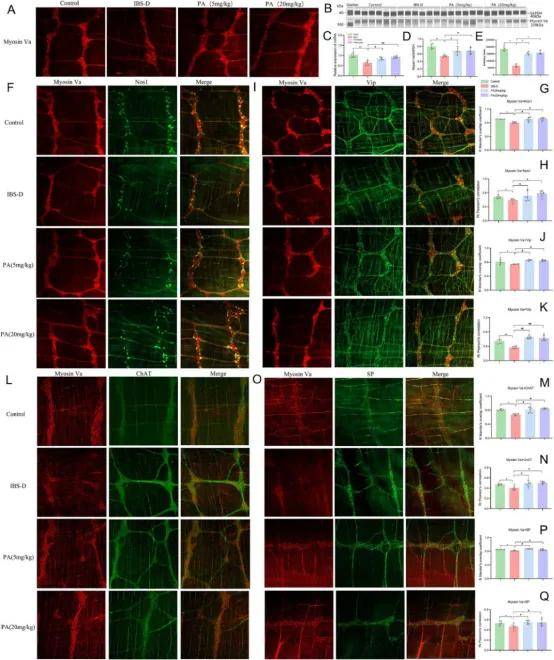
图10
分离培养原代大鼠结肠LMMP神经元观察myosin Va与抑制性和兴奋性神经递质相关蛋白的共定位。典型神经元在分离后第3天开始出现,显示形态生长并形成两个或多个突触建立神经纤维网络和神经节(图11A)。同时,β-tubulinIII和MAP-2免疫荧光证实培养物的神经元特性(图11B)。myosin Va与nNOS、动力蛋白轻链8(LC8)、SLC17A9、VIP、SP和ChAT等多种靶蛋白在肠神经元内显著共定位,主要表达在胞体和轴突,胶质细胞显示相应表达(图11C-F)。
IBS-D大鼠观察到的肠道推进增加可能归因于myosin Va向nNOS、VIP、ChAT和SP神经小泡转运减少,导致抑制性和兴奋性神经递质释放改变。PA提高myosin Va mRNA和蛋白水平,增加myosin Va与神经递质共定位,调节myosin Va向nNOS、VIP、ChAT和SP神经小泡转运,影响抑制性和兴奋性神经元功能,恢复神经稳态和调节肠道运动。
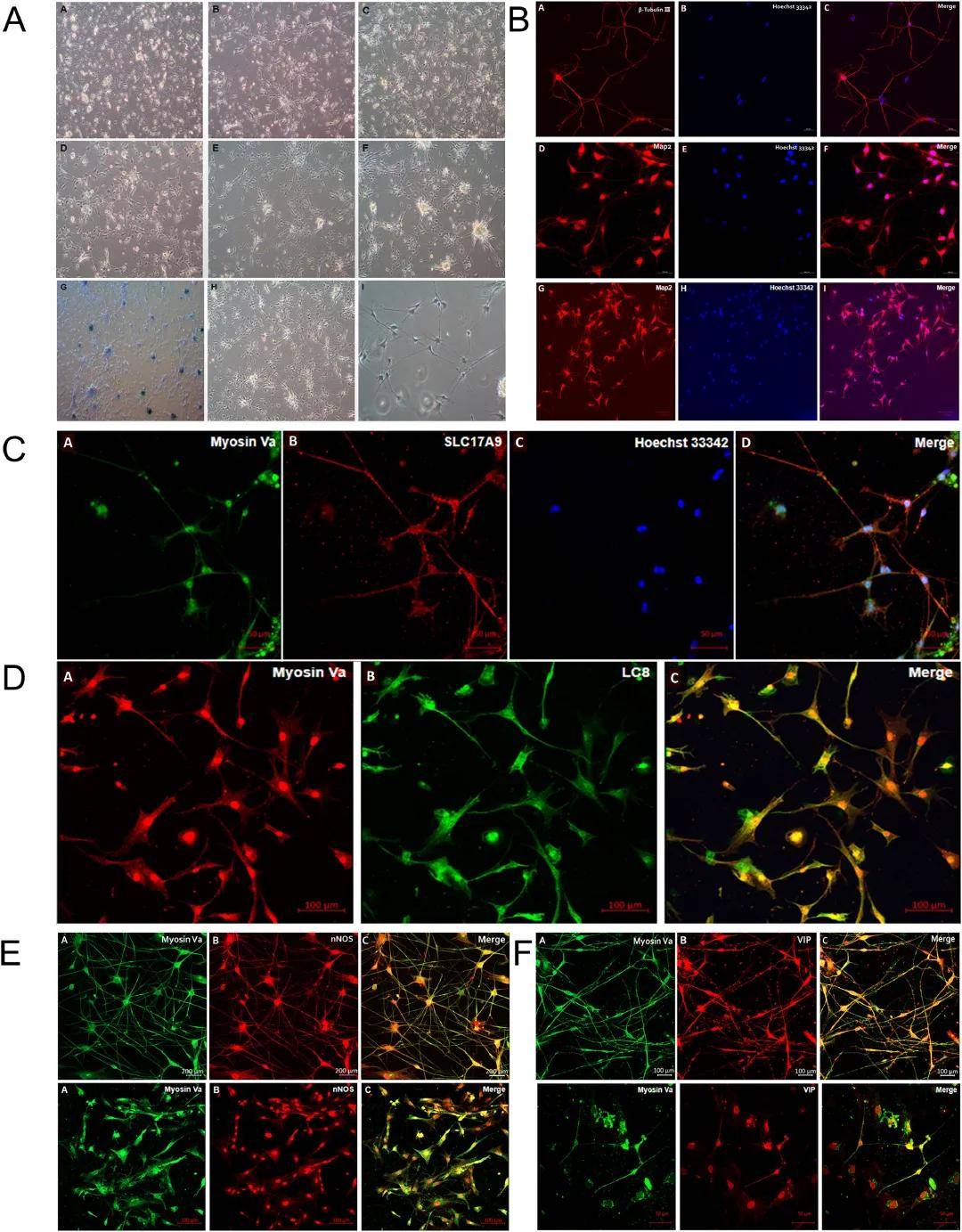
图11
9、PA对肌球蛋白Va基因缺陷DBA小鼠肠神经传导的影响
肌球蛋白Va基因缺陷的DBA小鼠表现出肠神经传导异常(图12A)。qPCR证实DBA小鼠中myosin Va基因表达。与C57BL/6J小鼠相比,DBA小鼠结肠组织中myosin Va mRNA相对表达显著降低(图12B)。
体外实验表明,与C57BL/6J小鼠结肠相比,DBA小鼠结肠对KCl的反应无显著差异。由于KCl直接影响平滑肌,结肠平滑肌无明显变化(图12I,J)。此外,与C57BL/6J小鼠结肠相比,DBA小鼠远端结肠对CCh的反应显著增强(图12C)。DBA小鼠结肠对EFS的舒张幅度增强,但这种反应在不同节段有差异。远端结肠对EFS的舒张反应减弱(图12F,G),而近端结肠对EFS的舒张反应增强(图12D,E)。这些结果表明在缺乏myosin Va的情况下,远端结肠抑制性神经传导活性降低,导致兴奋性神经传导占优势,表现为平滑肌收缩增强和舒张减弱。
随着PA浓度增加,缓解C57BL/6J和DBA小鼠结肠基础张力,同时降低自主结肠收缩频率(图12H)。100μMPA降低C57BL/6J和DBA小鼠远端结肠KCl诱导的收缩(图12I,J)。这些结果与早期体外研究一致,表明PA显著抑制IBS-D大鼠结肠平滑肌KCl诱导的峰值收缩张力。此外,100μMPA有效降低CCh诱导的结肠收缩张力,对DBA小鼠远端结肠CCh触发收缩表现出显著抑制作用(图12K,l)。
在C57BL/6J小鼠中,100μML-NAME显著抑制EFS诱导的结肠平滑肌舒张,同时增强EFS诱导的结肠平滑肌后收缩。此外,100μMPA降低C57BL/6J小鼠结肠对EFS和EFS+L-NAME诱导的后收缩(图12M-P)。这些结果与大鼠结肠平滑肌体外分析一致,表明PA(100μM)显著抑制氮能神经传导阻断后L-NAME诱导的后收缩。
DBA小鼠基线EFS收缩幅度显著低于C57BL/6J小鼠。在DBA小鼠中,100μMPA对平滑肌收缩幅度无显著影响。然而,添加L-NAME显著增强DBA小鼠平滑肌收缩幅度,作用模式与C57BL/6J小鼠相似,表明DBA小鼠氮能神经传导仍具功能(图12Q-T)。因此,当氮能神经传导被有效抑制时,EFS诱导的平滑肌舒张减弱,后收缩增强。关于L-NAME阻断氮能神经传导,PA降低平滑肌收缩幅度,但未达到DBA小鼠观察到的基线水平,表明PA对平滑肌的作用部分依赖于氮能神经传导。在缺乏myosin Va的情况下,PA无法发挥其对氮能神经传递的调节影响,表明PA对神经传递的调节依赖于myosin Va。
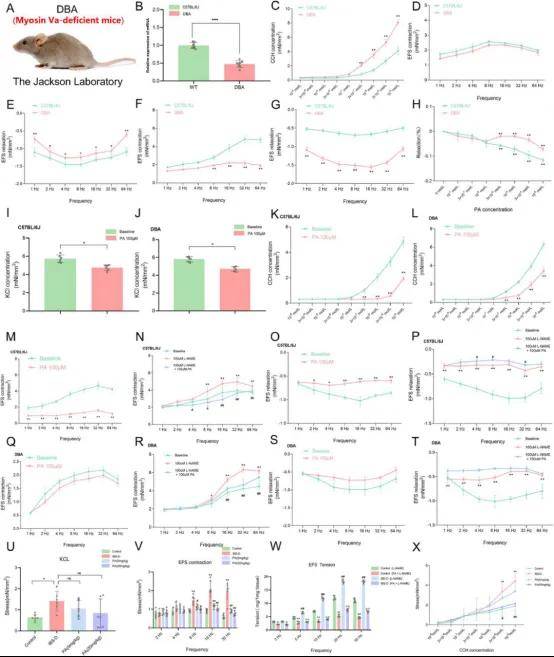
图12
10、肠神经元细胞肌球蛋白va功能缺失对PA调节作用的影响
为验证上述实验的意义,在动物模型中验证了肠神经元基因功能。转染后,将对照siRNA试剂(5cy3,红光)应用于神经元8小时,荧光显微镜观察拍照(图13A)。各siRNA组myosin Va mRNA相对表达水平显著低于对照组(图13B)。免疫荧光显示siRNA1组myosin Va荧光强度显著降低(图13C)。但siRNA1组与PA+siRNA1组间无明显差异(图13D,E),支持PA对myosin Va的调节可能发生在转录前或转录水平的结论。
PA对myosin Va和SLC17A9共定位的影响显示,siRNA1组Pearson相关系数和Mander重叠系数较对照组显著降低。同样,siRNA1组与PA+siRNA1组间这些系数无显著差异(图13F-H)。qPCR显示siRNA转染后,肠神经元myosin Va表达及抑制性神经递质相关蛋白水平较空白组显著下调。相比之下,与模型组相比,PA孵育后myosin Va mRNA相对表达水平增加,PA给药后各组相对表达水平增加(图14D,E)。
LC8是动力蛋白复合体组分,作为nNOS抑制剂。与nNOS结合后,LC8破坏nNOS二聚体稳定性,诱导其失活。除与nNOS相互作用外,LC8还与myosin Va相关,myosin Va是连接这两个实体的衔接蛋白(图13I-K)。人和小鼠SLC17A9基因编码蛋白作为囊泡核苷酸转运体,转运ATP、ADP和GTP等核苷酸。最近SLC17A9染色技术进展使肠神经元中扩张嘌呤能小泡的特异性鉴定成为可能。在myosin Va缺陷DBA小鼠中,SLC17A9和myosin Va的邻近连接分析信号缺失,扩张膜的外吐进入率降低(图13L-N)。
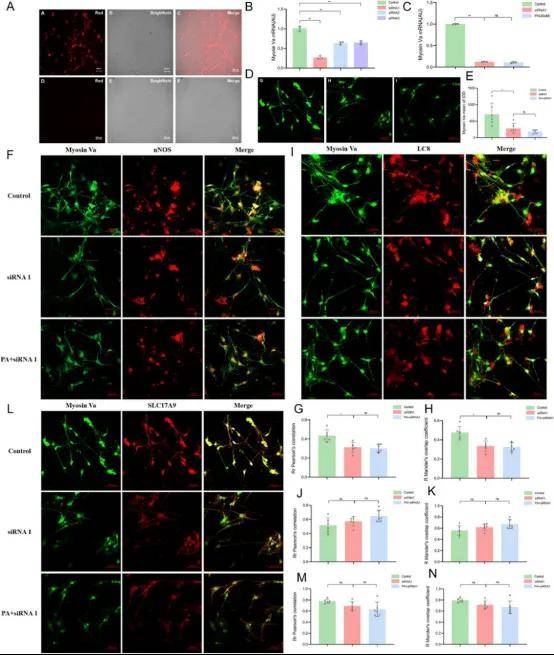
图13
11、肌球蛋白Va基因在鼠结肠神经元中过表达对PA调节作用的影响
分离培养原代肠神经元细胞,MAP2和TUJ免疫染色评估(图14A,B)。除抑制性神经递质外,免疫荧光显示myosin Va(红色)、SP(绿色)和ChAT(绿色)在原代大鼠结肠神经元中主要重叠,但两种共定位间存在明显差异(图14C)。siRNA转染后,肠神经元myosin Va、SP和ChAT mRNA较空白组显著下调(图14F)。相比之下,PA孵育后,与模型组相比myosin Va mRNA相对表达水平增加,PA给药后各组SP和ChAT mRNA增加(图14G)。
利用CAS9Easylentivirus技术,插入了一段完整的鼠肌球蛋白Va合成序列,并构建了肌球蛋白Va过表达lentiviral病毒载体(gRNA1、gRNA2和gRNA3)。转染组和对照组均表现出绿色荧光蛋白的表达,而空白对照组未显示荧光染色(图14H)。这一结果表明gRNA成功转染入神经元。转染后,每个gRNA组中的肌球蛋白Va水平显示出相对mRNA表达水平高于对照组,且gRNA2与gRNA3之间观察到统计学显著差异(图14I)。qPCR显示,与对照组相比,gRNA3组的肌球蛋白VamRNA表达水平显著增加;然而,gRNA3和PA+gRNA3组无显著差异。免疫荧光显示,与对照组相比,gRNA3组的肌球蛋白Va荧光强度显著升高,gRNA3和PA+gRNA3组无显著差异(图14J和K)。初步结果表明,PA对IBSD大鼠结肠组织中的肌球蛋白Va基因转录和蛋白水平具有上调作用。这个基因过表达模型中,PA未诱导肌球蛋白Va表达的下调,表明PA和gRNA3过表达载体对该基因具有相同的调控方向,PA具有良好的药物能力,且可能不会引起显著的临床副作用。
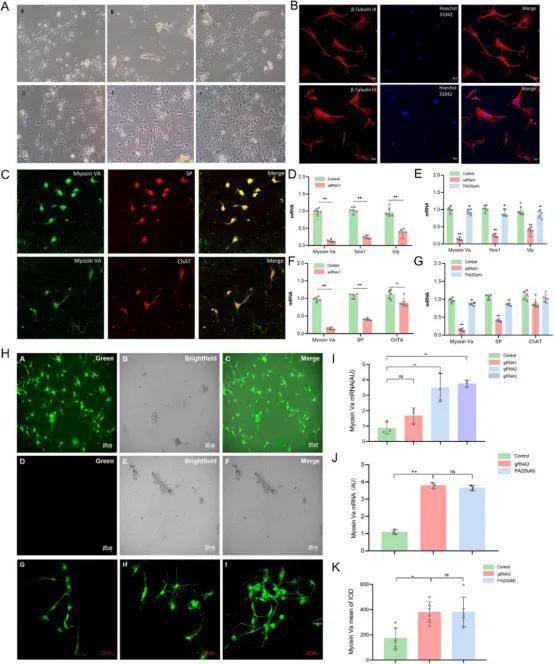
图14
总结:PA以MYO5a为核心靶点,重塑ENS兴奋-抑制神经元平衡,恢复肠道动力与菌群稳态,为IBS-D提供了安全、可转化的中医药新策略。傲星生物深耕生信分析十余载,有丰富的实验方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




