IF:15.7,单细胞多组学+自噬+棕榈酰化+动物验证,解析心梗潜在治疗靶点!
题目:抑制CD36棕榈酰化通过调节脂质代谢稳态和自噬改善心肌梗死后心脏功能
英文名:Inhibiting CD36 palmitoylation improves cardiac function post-infarction by regulating lipid metabolic homeostasis and autophagy
杂志:Nature Communications
影响因子:15.7
发表时间:2025年7月17日
研究背景:心肌梗死(MI)后,心肌能量底物代谢改变和线粒体损伤导致心脏结构和功能异常。脂肪酸转运蛋白CD36在调节脂质稳态和线粒体代谢中起关键作用,但其棕榈酰化修饰在MI中的功能尚未明确,故探究其对MI后心脏功能的影响及机制。
研究思路:通过建立小鼠MI模型,结合蛋白质组学、代谢组学和单细胞RNA测序解析MI后心肌代谢和线粒体功能变化,聚焦CD36的作用;再通过药物干预(如SSO)、基因编辑(CD36敲除、棕榈酰化位点突变)等手段,研究CD36棕榈酰化对其亚细胞定位、脂质代谢、自噬及心脏功能的影响,阐明其通过调节细胞膜CD36介导的脂肪酸摄取及线粒体CD36-PGAM5轴调控自噬的分子机制。
研究结果:
1、蛋白质组学分析揭示心肌梗死后的代谢重编程和线粒体功能障碍
通过结扎左冠状动脉4周建立小鼠心肌梗死(MI)模型,对假手术小鼠和缺血损伤小鼠的心脏组织进行蛋白质组测序(图1a、b)。共鉴定出3490种蛋白质,包括112种上调和195种下调(图1c)。差异表达蛋白GO富集表明,下调蛋白主要与能量生成相关过程有关,如“ATP代谢过程”“氧化磷酸化”和“电子传递链”(图1d)。KEGG分析显示MI中代谢通路显著减少,包括“柠檬酸循环(TCA循环)”“碳代谢”“代谢通路”和“氧化磷酸化”,特别是“NF-κB信号通路”和“铁死亡”(图1e)。在物质代谢通路中,脂肪酸代谢受影响较大,几乎所有与“脂肪酸代谢”“脂肪酸降解”和“脂肪酸延长”相关的蛋白在MI中丰度约降低两倍(图1f)。差异蛋白亚细胞定位表明差异蛋白主要定位于线粒体,几乎所有参与氧化磷酸化、TCA循环和核糖体的蛋白均显著下调(图1g-h)。
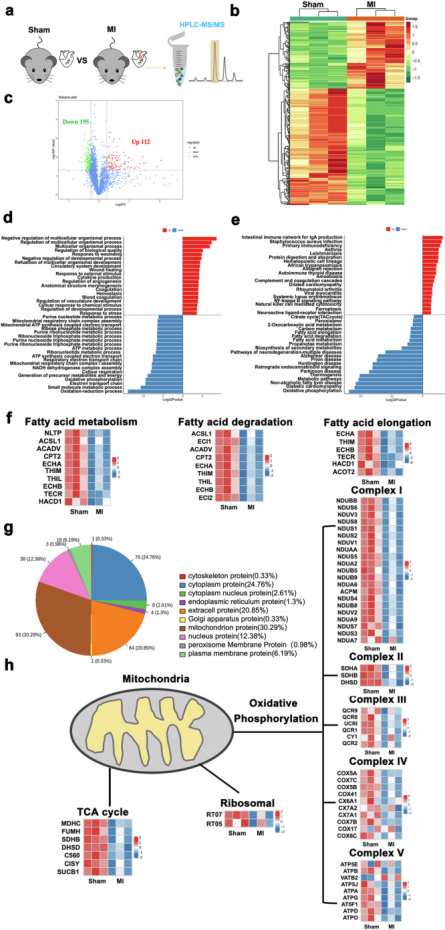
图1
2、心肌梗死后心肌中脂毒性代谢物的积累
qRT-PCR验证了蛋白质组学结果(图2a、b)。分离假手术和MI小鼠心脏线粒体,Westernblotting显示MI组线粒体电子传递链复合物表达变化(图2c)。MI使心肌神经酰胺、DAG显著升高(图2d、e),MDA升高、SOD降低,提示脂质过氧化和氧化应激增加(图2f、g)。PGC1αmRNA降低表明线粒体氧化代谢受损(图2h)。MicroPET/CT显示MI后4周心肌葡萄糖摄取减少,伴随Glut4膜定位减少(总蛋白不变)(图2i、j)。综上,MI后心脏糖脂代谢紊乱,与线粒体氧化能力下降导致有害脂质升高有关。

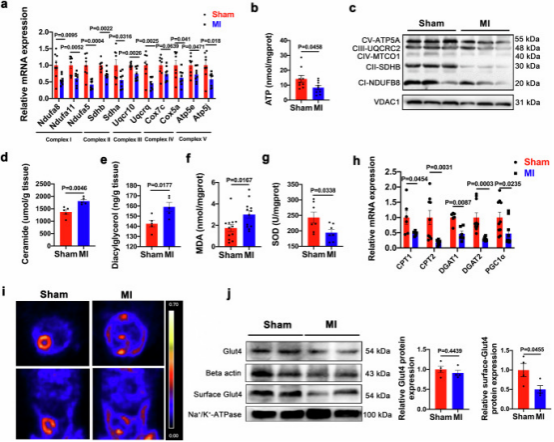
图2
3、单细胞RNA测序鉴定CD36为心肌细胞代谢的关键调控因子
为深入了解MI后心肌代谢重塑的潜在机制并探索跨细胞类型的分子机制进行了单细胞RNA测序(图3a)。基于标记基因Pln和Slc8a1鉴定心肌细胞(图3b)。通过这种方式,鉴定出假手术组和MI组心肌细胞中452个差异表达基因,其中214个上调,238个下调(图3c)。联合蛋白质组学和心肌细胞转录组测序数据,有34个基因在两个数据集中均富集(图3d)。GO和KEGG富集分析显示,重叠的下调基因在电子传递链和氧化磷酸化通路中富集,表明线粒体功能不仅在翻译后水平而且在转录水平受到抑制(图3e、f),在上调基因中,至少鉴定出三个与脂肪酸代谢相关的基因,即CD36、Fabp4和Fabp5,如UMAP图所示(图3g)。

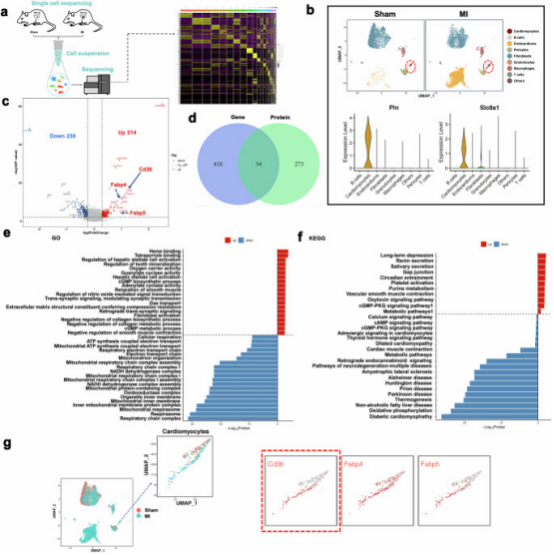
图3
通过WB实验验证单细胞测序结果中CD36蛋白的表达。结果表明,与单细胞测序结果不同,假手术组和MI组心肌组织总蛋白中CD36水平相对不变(图4a)。推测心肌组织由多种细胞类型组成,心肌细胞内CD36表达的变化可能被样本中其他细胞类型的基因表达谱所掩盖。为验证这一假设,从假手术组和MI组中分离成年小鼠心肌细胞,通过PCR和Western Blot分析评估CD36水平的变化。结果表明MI组中CD36 mRNA表达显著增加(图4b);然而,总CD36蛋白水平并未随mRNA表达相应增加(图4c)。共聚焦显微镜分析进一步证实了这一发现,显示MI小鼠心肌细胞细胞膜上的CD36水平升高(图4d)。
总之,多组学数据的整合提供了对MI中转录后和翻译后调控更全面的理解,CD36成为调节MI后心肌细胞代谢过程和线粒体功能的潜在分子靶点。

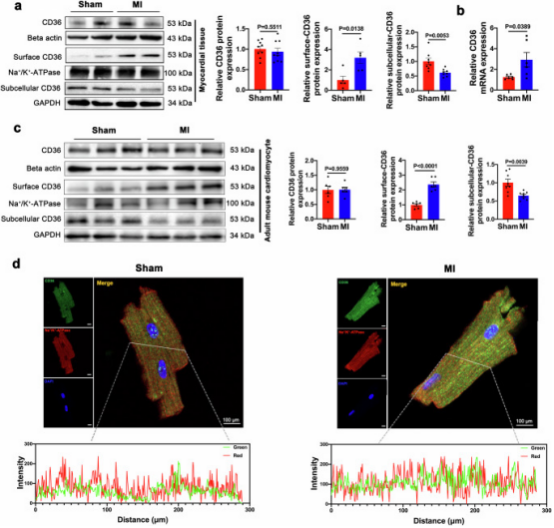
图4
4、抑制CD36介导的脂肪酸摄取通过减小梗死面积和改善代谢来改善心脏功能
为确定抑制CD36能否保护心脏免受缺血损伤,对MI模型C57BL/6小鼠每周腹腔注射40mg/kg SSO或溶剂,持续4周(图5a)。结果显示,SSO处理显著改善左心室射血分数和缩短分数,减轻MI影响(图5b),TTC染色显示其显著减小梗死面积(图5c)。H&E和Masson染色证实,SSO减轻了MI后心肌纤维紊乱、纤维组织及胶原沉积(图5d、e);TEM显示其减轻心肌超微结构损伤,减少细胞水肿,保留线粒体基质(图5f)。此外,SSO处理显著降低MI诱导的心肌神经酰胺、DAG水平及MDA含量,升高SOD水平,改善脂质谱和脂质过氧化(图5g-j)。

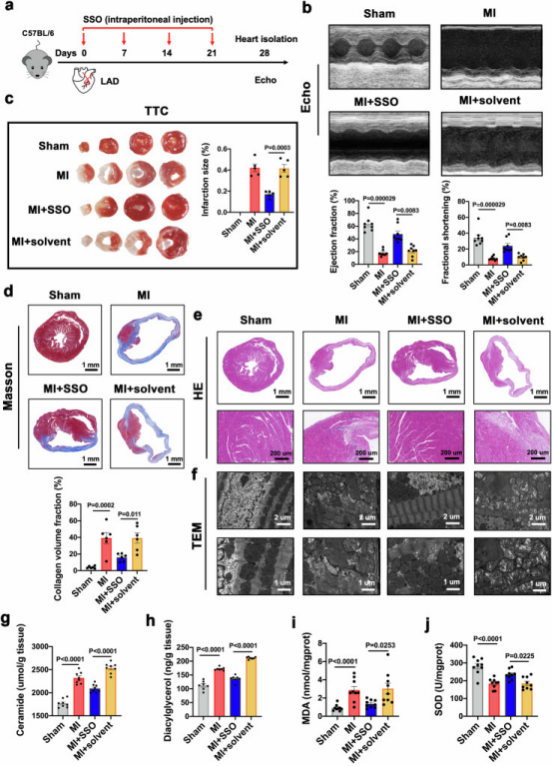
图5
5、棕榈酰化是CD36细胞膜定位和细胞脂肪酸摄取活性所必需的
研究MI后CD36细胞膜定位增强的机制发现,MI心脏中CD36棕榈酰化水平显著升高(图6a)。用PA诱导或2bp抑制棕榈酰化后,PA显著增加CD36棕榈酰化及细胞膜定位,总CD36水平无明显变化,表明棕榈酰化调节CD36亚细胞转运(图6b、c)。双变量流式细胞术显示,PA增强心肌细胞脂肪酸结合与摄取,且依赖CD36表面表达(图6d、e),说明CD36棕榈酰化通过调节其定位影响脂肪酸摄取。缺氧还增加脂肪酸摄取及毒性脂质,PA放大、2bp减轻该效应(图6f-l)。综上,抑制CD36棕榈酰化可通过改变其细胞膜定位减轻缺氧诱导的心肌细胞毒性脂质积累。

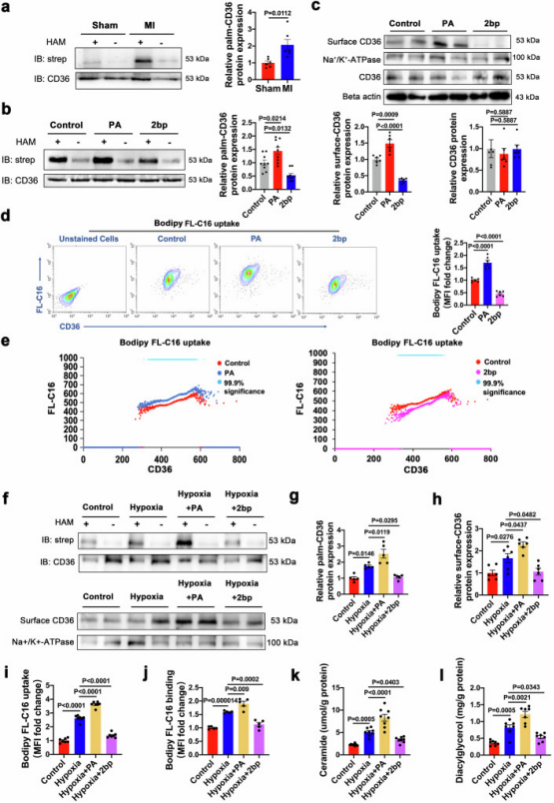
图6
构建了AA-SS25突变体质粒(4个半胱氨酸被替换),转染心肌细胞后,与WT-CD36组相比,AA-SS-CD36组细胞膜CD36降低、亚细胞CD36升高(图7a、b)。双色流式细胞术显示其脂肪酸结合和摄取显著减少,且依赖CD36表面表达(图7c、d)。缺氧条件下,AA-SS-CD36恢复神经酰胺和DAG水平(图7e、f),改善线粒体呼吸(OCR),降低mtROS(图7g、h)。综上,棕榈酰化对CD36的定位和脂肪酸摄取活性关键,其突变可减轻缺氧损伤,具改善MI后梗死面积的潜力。

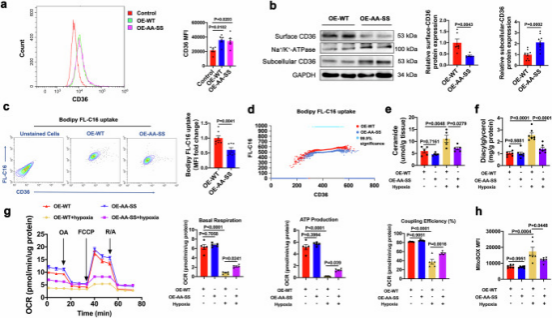
图7
6、抑制CD36棕榈酰化减轻心肌梗死诱导的心脏损伤
为确定CD36棕榈酰化在MI后心脏损伤中的作用,用CRISPR/Cas9生成CD36敲除小鼠,借助带cTNT启动子的AAV9系统实现心肌细胞特异性过表达WT-CD36和AA-SS-CD36,注射到CD36KO小鼠中。证实敲除和过表达效果后,发现AA-SS型使膜上CD36减少、亚细胞CD36增加,改善心功能(EF、FS升高),减少纤维化和脂质损伤,降低MDA等,升高SOD(图8)。总之,结果表明,抑制CD36棕榈酰化通过减小梗死面积和脂毒性代谢物、恢复线粒体功能并防止线粒体氧化能力受损后的脂质过载来增强心脏功能。

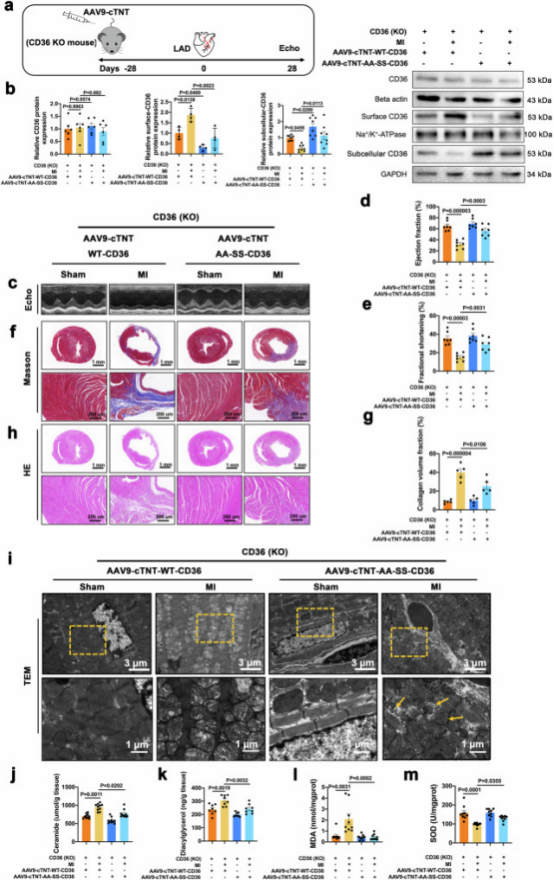
图8
7、CD36棕榈酰化抑制防止PGAM5的泛素化和降解并促进线粒体自噬
先前研究证实自噬可保护MI损伤,MI后心肌自噬减少(SQSTM1升高、LC3B-II降低。本研究发现,CD36棕榈酰化抑制(CD36KO-AA-SS-CD36)使MI后自噬结构积累更多,自噬水平升高(LC3B-II升高、SQSTM1降低),心肌细胞中亦如此(图8i、9a、b)。用雷帕霉素、氯喹处理,抑制CD36棕榈酰化均增加自噬体形成。自噬拮抗剂3-MA减弱其治疗效果,表明其通过促进自噬保护MI后心脏功能。为探索CD36棕榈酰化抑制调节自噬的下游介质,经数据库分析和互作筛选,鉴定出PGAM5为关键因子(图9c)。验证显示CD36与PGAM5相互作用,棕榈酰化抑制增强该作用(图9d),且PGAM5是其诱导自噬所必需(图9e)。
抑制CD36棕榈酰化促进CD36线粒体定位,增加线粒体中CD36和PGAM5水平(图9f-h),通过减少PGAM5泛素化增强其稳定性(图9j、k),进而降低Fundc1和Drp1(S637)磷酸化,激活线粒体自噬(图9l)。线粒体自噬拮抗剂Mdivi-1减弱其功能改善效果,证实其依赖性。

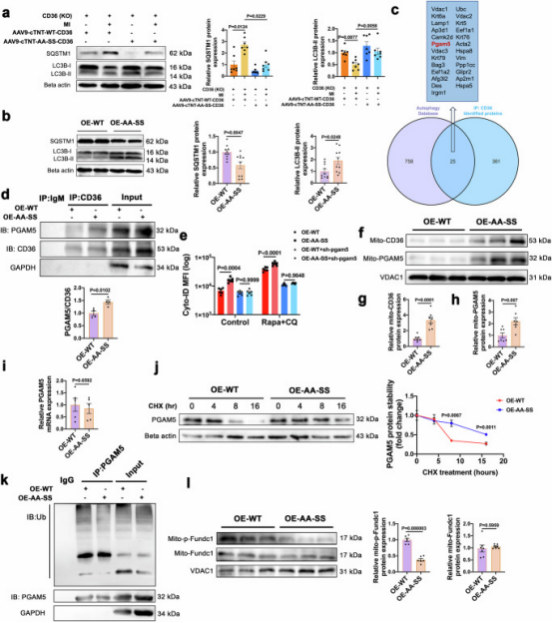
图9
总结:研究发现抑制CD36棕榈酰化可减少细胞膜CD36介导的脂肪酸过载,同时增强线粒体CD36-PGAM5信号轴活性以调节自噬,从而改善MI后心脏功能,为MI治疗提供了新的潜在靶点。
傲星生物深耕生信分析十余载,有丰富的实验方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




