IF:8.1,卵巢癌+GJB2+铜死亡+细胞实验与生信分析,揭示新型预后标志物,助力精准治疗突破!
题目:GJB2作为一种新的与卵巢癌免疫浸润和铜增生相关的预后生物标志物
英文名:GJB2 as a novel prognostic biomarker associated with immune infiltration and cuproptosis in ovarian cancer
杂志:Apoptosis
影响因子:8.1
发表时间:2025年5月15日
研究背景:卵巢癌死亡率高,早期诊断难、易耐药复发,缺乏可靠预后标志物;铜死亡与癌症相关,但在卵巢癌中机制不明,GJB2在其他癌症有作用,其在卵巢癌中的功能及机制尚未明确。
研究思路:首先从公共数据库收集卵巢癌相关数据,筛选差异表达的铜死亡相关基因,通过Cox回归和LASSO算法构建含5个CRGs的预后模型并验证,随后聚焦与铜死亡基因关联最多的GJB2,通过细胞实验探究其在卵巢癌细胞增殖、迁移、EMT、铜死亡及免疫浸润中的作用及机制。

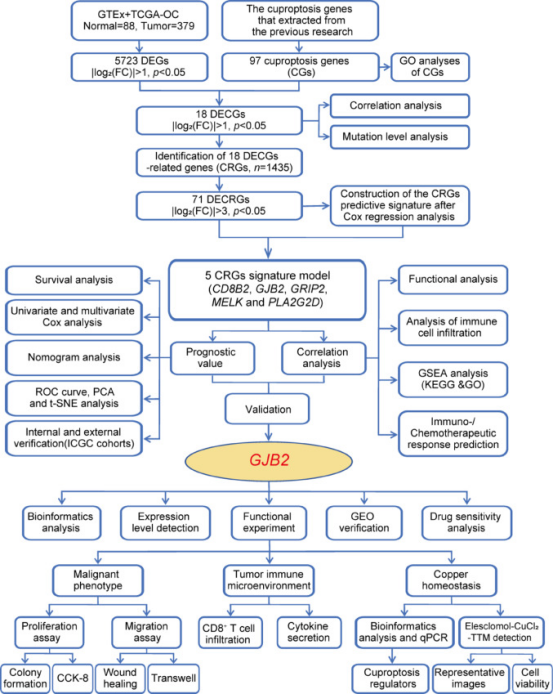
图1
研究结果:
1、DECGs和卵巢癌患者的分子特征
为探究铜死亡相关基因(CRGs)与卵巢癌的相关性,从已发表文献收集97个铜死亡基因(CGs)。通路富集分析显示其与多种铜信号通路显著相关(图2A)。随后比较正常卵巢组织和卵巢癌样本,鉴定出5723个差异表达基因(DEGs)(图2B)。97个CGs中有18个在TCGA队列差异表达(图2B),其中8个差异表达铜死亡基因(DECGs)上调、10个下调,表明卵巢癌中铜死亡失调(图2C)。对18个DECGs表达相关性分析,显示铜死亡调控因子关联高度一致(图2D)。
接着分析18个DECGs体细胞突变频率,发现462个卵巢癌样本中有56个(12.12%)存在这些基因突变,主要为错义突变(图2E)。评估DECGs的体细胞拷贝数变异(CNVs),发现所有18个基因均存在广泛CNVs,卵巢癌患者中DECGs的CNVs频率见图2F,这些基因改变的CNVs的染色体位置见图2G。最后,Pearson相关性分析显示,1453个CRGs与18个DECGs显著相关(图2H),其中1453个CRGs中鉴定出71个差异基因,包括肿瘤组织中30个上调、41个下调的CRGs(图2I)。

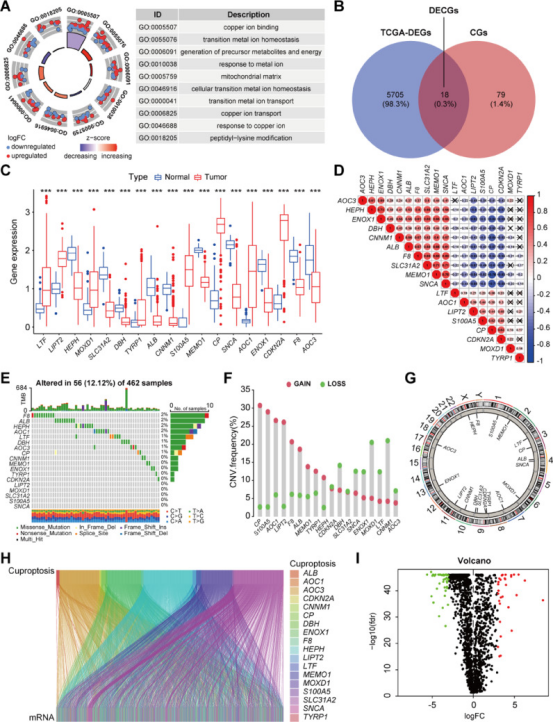
图2
2、铜死亡相关预后模型的构建与验证
对71个crg的单变量Cox回归分析、LASSO回归分析从而选择5个crg用于风险评分模型的开发(图3A)。图3B显示了说明18个DECGs和5个crg之间关系的热图。采用KM法比较两组患者的OS,结果显示高危组患者的OS明显差于低危组(p=0.003,图3C)。在单变量Cox分析中,年龄和风险评分均显示与OS具有统计学显著相关性(p<0.001,图3D)。此外,在多变量Cox回归分析中,两个变量都保留了它们对OS的预后意义(图3E)。5个关键风险评分基因的表达水平在高风险组和低风险组之间存在显著差异(图3F)。具体来说,GRIP2、GJB2和CD8B2在高危人群中表达更高,而PLA2G2D和MELK的表达水平较低(图3F)。3组(all组、训练组和测试组)的散点图表明,OC患者的死亡率随着风险评分的升高而增加(图3F)。受试者操作特征(ROC)曲线分析显示,用于评估OC患者1年、2年和3年生存结果的曲线下面积(AUC)值均大于0.5,证明了预测模型的高特异性和敏感性(图3G)。三维主成分分析(PCA)显示,基于18个DECGs和所有CRGs表达组,高风险和低风险患者的分布是不可区分的(图3H,I)。然而,基于5个crg的高风险和低风险组的分布是最明显的(图3J)。总的来说,这些发现表明,基于5个基因的预后风险模型可以作为OC预后的可靠预测因子。

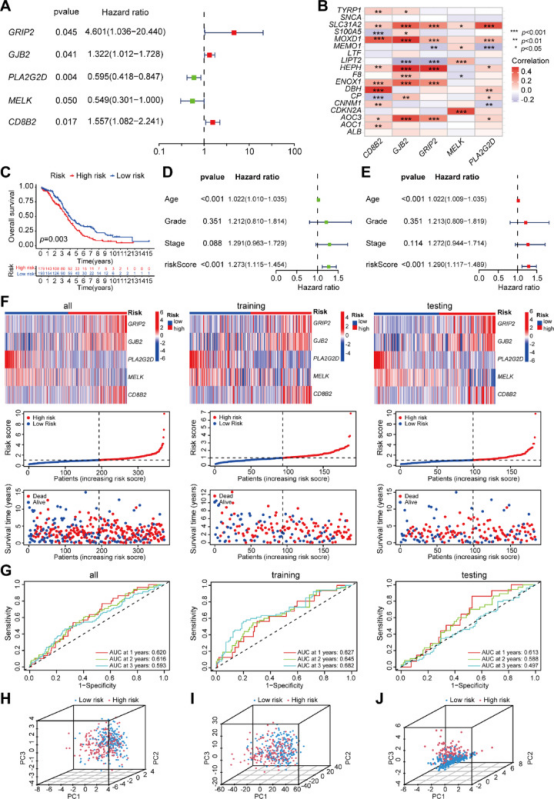
图3
3、TCGA和ICGC队列中5个CRGs风险模型的预后分析
预后风险评分结合年龄和肿瘤分级生成ROC生存曲线。结果显示,与其他临床特征相比,CRGs预后风险评分系统能准确预测OC样本1年、3年和5年生存率(图4A - C)。利用5个CRGs特征构建预测nomogram预测1年、3年和5年OS概率,如图4D所示,各因素评分对应其对生存风险的贡献。校准曲线验证nomogram准确性,实际值与预测值高度吻合(图4E)。此外,风险评分的c指数大于0.5,表明风险模型在预测OC患者OS方面有显著优势(图4F)。为评估基于5个CRGs的风险模型分类能力,对所有TCGA数据集进行主成分分析(图4G)和t分布随机邻居嵌入(t - SNE)(图4H),结果显示高、低风险组分布明显,预后特征可准确区分(图4G,H)。另外,将CRGs特征预后模型与TIDE模型和TIS模型比较,发现该模型预测OC样本1年生存率的能力更好(图4I)。

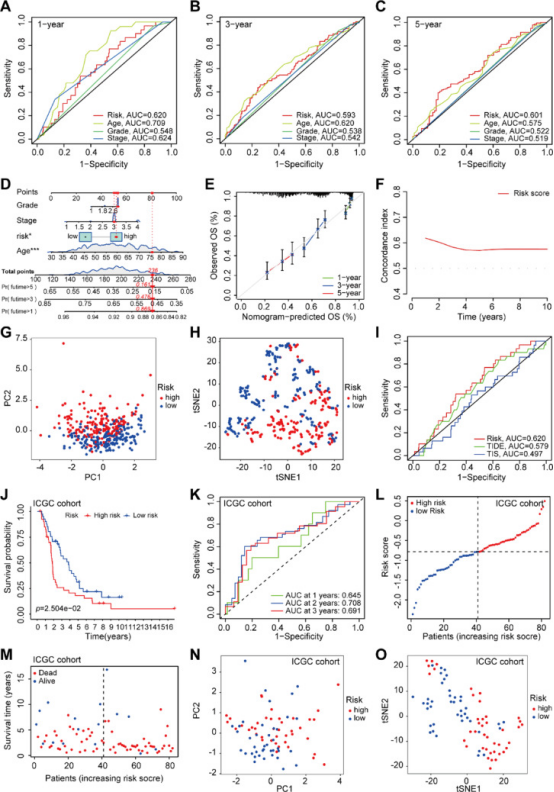
图4
4、铜死亡相关基因风险评分预测信号通路、肿瘤微环境和免疫细胞浸润
利用KEGG和GO数据库进行基因集富集分析(GSEA),探究由5个CRG特征定义的高风险组和低风险组之间生物学功能和信号通路的差异(图5-A、B)。高风险组在ECM受体相互作用、黏着斑和WNT信号通路等通路中显著富集,而低风险组在趋化因子信号通路和原发性免疫缺陷相关通路中显著富集(图5-A、B)。使用CIBERSORT比较高风险组和低风险组的免疫细胞浸润情况(图5C)。为进一步评估风险评分对免疫治疗的预测价值,使用ESTIMATE算法评估卵巢癌细胞的免疫评分,发现低风险组具有更高的免疫评分(图5D),表明其肿瘤微环境具有更强的免疫活性。重要的是,对免疫排斥模式的分析显示,其与风险评分呈显著正相关(图5E)。Kaplan-Meier分析显示,高TMB组患者的OS显著优于低TMB组(p<0.001,图5F)。TMB和CRG风险评分的联合生存分析进一步显示,高TMB且低风险评分的患者预后最-佳,而低TMB且高风险评分的患者预后最差(图5G)。得出结论,低风险组患者更有可能从免疫治疗中获益。

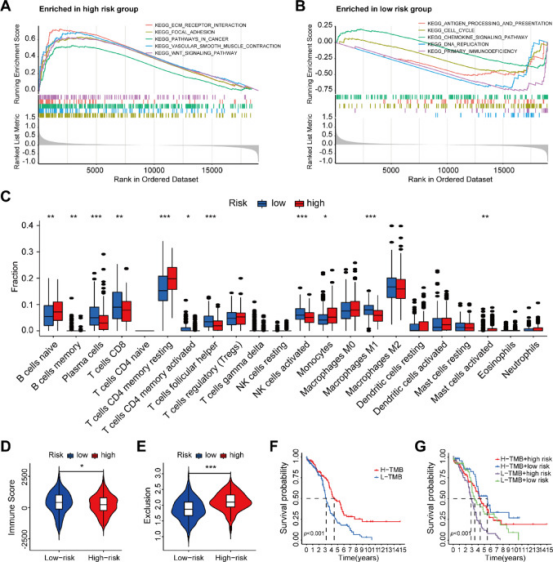
图5
5、高风险组和低风险组的免疫治疗分析和药物敏感性预测
对免疫检查点的分析结果表明,无论是单独使用抗CTLA-4和抗PD-1还是联合使用,低风险组患者对免疫治疗的反应更好(图6A-D)。这一发现进一步支持了假设,即风险评分可以预测免疫治疗的敏感性和疗效。

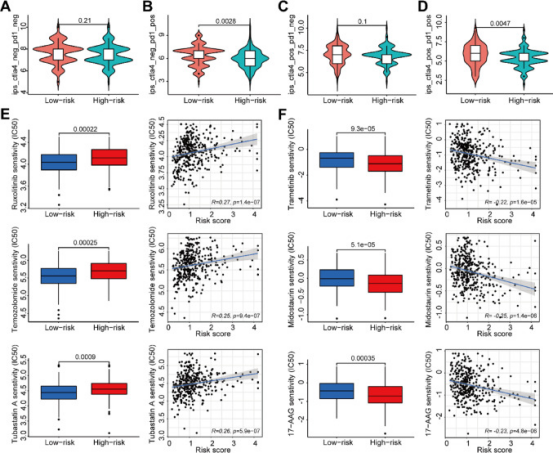
图6
6、GJB2在卵巢癌中的表达及生存预后分析
为进一步验证预后特征,通过体外实验进行了功能测定,GJB2与铜死亡基因的关联数量最多,并且与多个关键肿瘤相关信号通路呈显著正相关(图7A)。qPCR结果表明,与IOSE细胞相比,卵巢癌细胞系中GJB2表达显著更高(图7B)。与正常卵巢组织相比,肿瘤组织中GJB2表达水平显著升高(图7C)。IHC结果表明,与正常卵巢组织相比,卵巢癌组织中GJB2蛋白表达上调(图7D),这证实了基于qPCR的观察结果,并进一步支持GJB2在卵巢癌发展中的潜在致癌作用。
通过对多个独立队列的综合生物信息学分析(图7E),一致观察到与正常对照组相比,卵巢癌组织中GJB2表达显著上调,TCGA+GTEx(图7E-J)数据集中使用ROC曲线下面积(AUC)评估了GJB2的诊断性能。。在TCGA-卵巢癌数据集中,GJB2高表达与较差的OS结果相关(图7K)。除OS外,GJB2高表达还与较差的无进展生存期(PFS)结果相关(图7L-M)。为进一步探究GJB2表达与卵巢癌预后的关系,在GEO数据集队列(GSE63885)中评估了其预后意义。荟萃分析证实,GJB2是一个独立的预后因素,高表达与卵巢癌患者的不良预后相关(图7N)。此外,使用ROC分析评估了GJB2在GSE63885队列中区分肿瘤和正常样本的诊断效用。ROC曲线显示,预测患者1年、3年和5年生存率的AUC值均大于0.5(图7O)。GJB2表达与几种化疗药物的敏感性呈负相关,包括阿法替尼、西妥昔单抗、多西他赛、吉非替尼和曲美替尼(图7P)。

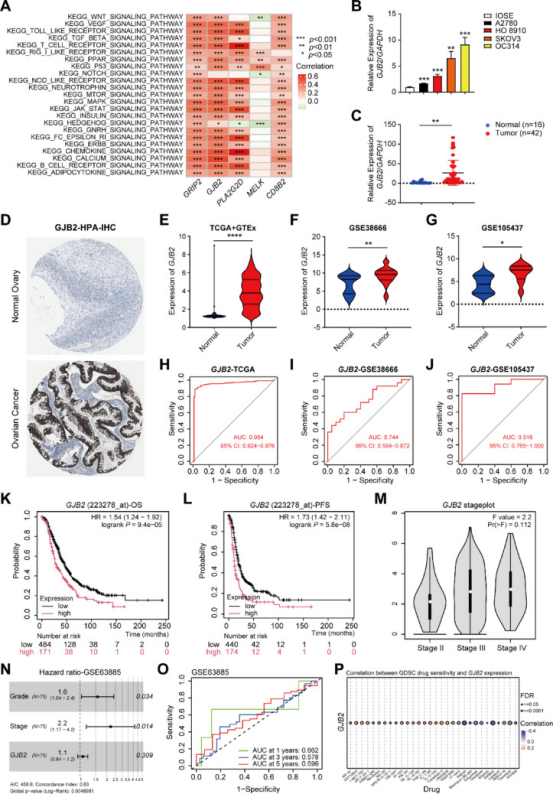
图7
7、GJB2调节卵巢癌细胞的恶性表型和EMT
本研究发现,SKOV3和OC314细胞中GJB2表达高于A7820和HO8910细胞(图7B);选敲低效率有效的GJB2-si2/3(图8A)处理后,SKOV3/OC314细胞的增殖(图8B-C)和迁移均显著降低,提示沉默GJB2可抑制卵巢癌细胞增殖迁移。 构建GJB2过表达(GJB2-OE)质粒转染HO8910/A2780细胞,qPCR/Western blotting证实GJB2显著升高(图8F);且GJB2-OE可促进细胞增殖(图8G-H)、提高迁移率(图8I-J),表明靶向GJB2或为卵巢癌潜在治疗策略。生物信息学分析显示,GJB2高表达的卵巢癌样本中EMT相关通路显著富集(图8K);实验进一步证实,GJB2过表达可下调上皮标志物E-钙粘蛋白,上调间充质标志物N-钙粘蛋白/波形蛋白(图8L-M),提示GJB2可能通过激活EMT促进卵巢癌转移。

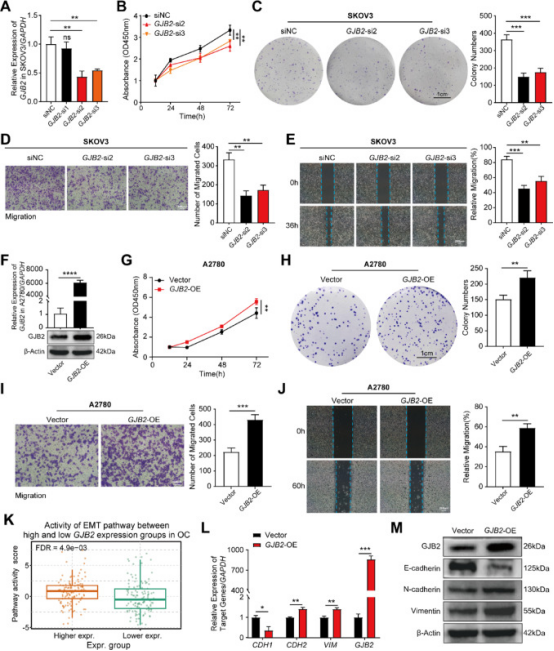
图8
8、GJB2与铜离子载体诱导的细胞死亡相关
GJB2相关基因GO富集于铜离子结合通路(图9A);GJB2过表达下调卵巢癌细胞铜死亡核心调控因子(图9B),提示其参与铜死亡调控。elesclomol-CuCl2(1:1)处理HO8910/A2780细胞24h的IC50为30nM/15nM(图9C-D);铜螯合剂TTM可挽救其诱导的细胞死亡(图9E-F),证实该死亡依赖铜积累。GJB2过表达(GJB2-OE)显著升高elesclomol-CuCl2处理后的IC50值(图9G-H),且GJB2-OE组细胞活力高于Vector组(图9I-J),表明GJB2过表达减轻卵巢癌细胞的铜诱导死亡。

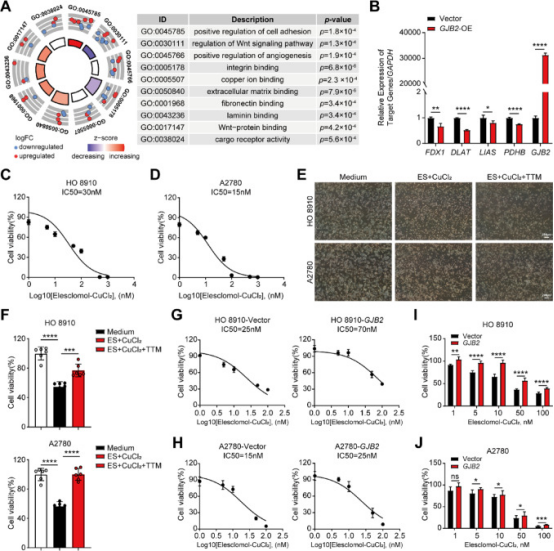
图9
9、GJB2抑制CD8+T细胞浸润并促进免疫逃逸
功能延伸研究显示,GJB2相关基因GO富集于铜离子结合通路(图9A);GJB2过表达显著下调卵巢癌细胞中铜死亡核心调控因子(图9B),提示GJB2参与铜死亡调控。elesclomol-CuCl2(1:1)处理HO8910/A2780细胞24h的IC50分别为30nM/15nM(图9C-D);铜螯合剂TTM可挽救其诱导的细胞死亡(图9E-F),证实该死亡依赖铜积累。 GJB2过表达显著升高elesclomol-CuCl2处理后的IC50值(图9G-H),且GJB2-OE组细胞活力显著高于Vector组(图9I-J),表明GJB2过表达可减轻卵巢癌细胞的铜诱导死亡。

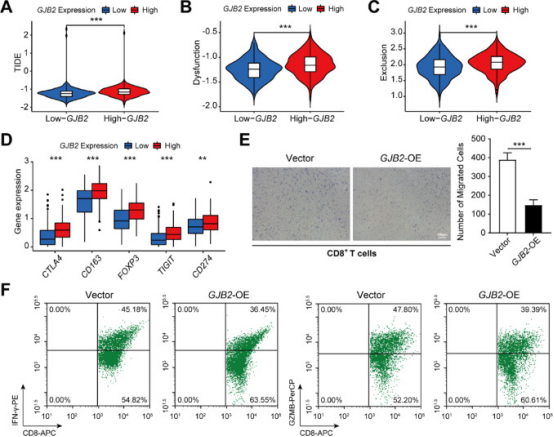
图10
总结:本研究构建了含5个CRGs的卵巢癌预后模型,验证其可靠性,发现GJB2在卵巢癌中高表达,通过调控增殖、迁移、EMT、铜死亡及免疫逃逸促进肿瘤进展,可作为预后生物标志物和治疗靶点。傲星生物深耕生信分析十余载,具有丰富的实验方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




