IF:5.9,生信套路解锁新疾病:多组学+机器学习双引擎驱动,3天出稿不是梦!
题目:基于分子亚型的免疫相关标记预测肝细胞癌预后和免疫治疗效果
英文名:An immune-related signature based on molecular subtypes for predicting the prognosis and immunotherapy efficacy of hepatocellular carcinoma
杂志:Frontiers in Immunology
影响因子:5.9
发表时间:2025年5月19日
研究背景:免疫治疗是包括肝细胞癌(HCC)在内多种恶性肿瘤的关键疗法。但HCC早期症状不特异、异质性显著,多数患者确诊时已晚期,无法根治手术,即便采用免疫和靶向治疗,5年生存率仍低于20%。目前基于RNA测序的预后评估模型操作复杂、成本高,而免疫组织化学(IHC)实用经济,因此亟需构建基于HCC分子亚型和免疫相关基因的预后模型,并通过IHC验证以促进临床转化,为精准免疫治疗提供指导。
研究思路:本研究先利用京都基因与基因组百科全书(KEGG)通路,通过基因集变异分析(GSVA)和共识聚类分析区分HCC分子亚型;在TCGA - LIHC队列中,结合免疫相关基因筛选出亚型特异性免疫相关差异表达基因(SIRDEGs)。随后,通过单变量、Lasso和多变量Cox回归分析构建亚型特异性免疫相关预后模型(SIR - PS),并在多个预后队列、一个免疫治疗队列、不同HCC细胞系和组织芯片中验证。同时,通过肿瘤微环境分析、突变分析、空间转录组分析、qPCR、Western blotting等实验探索模型临床意义及调控免疫治疗效果的潜在机制。最终,结合IHC染色评估模型在临床实践中的应用价值。

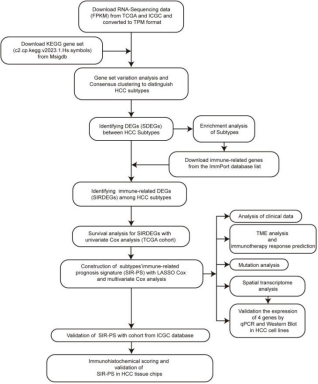
图1
研究结果:
1、基于KEGG通路的HCC亚型鉴定与富集分析
利用基于GSVA算法的KEGG基因集富集得分,对样本进行无监督层次聚类,将其分为两个不同亚型,并用聚类热图、共识CDF图、平均轮廓宽度和模糊聚类比例算法验证分类稳定性(图2A - C)。随后,比较分析不同亚型的临床因素,用热图可视化(图2D),并用堆叠柱状图突出显示亚型间有显著差异的因素(图2E)。与Sub2相比,Sub1特征是甲胎蛋白(AFP)水平升高、组织学分级更高、病理分期和T分期更晚、女性患者比例更高且中位年龄更低。Kaplan - Meier分析显示,Sub2患者预后优于Sub1患者(图2F)。对Sub1的富集分析显示,在四个数据库中,Sub1富集的基因均与免疫缺陷疾病相关(图2G)。此外,对亚型间免疫检查点表达水平的分析表明,Sub1中免疫检查点基因整体表达水平显著高于Sub2(图2H)。

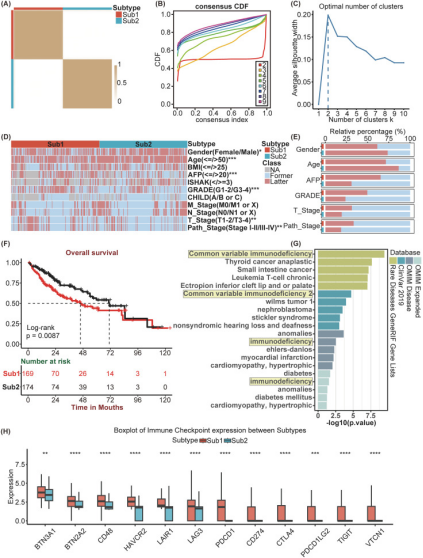
图2
2、SIR-PS模型的构建与验证
从TCGA-LIHC队列和ImmPort数据库获取239个免疫相关差异表达基因(图3A)。经单变量Cox和Lasso回归分析,最终筛选出5个关键SIRDEGs用于构建预后模型(图3B、C)。在TCGA队列中,按中位风险评分将患者分为高、低风险组,结果显示随风险评分上升,患者死亡率及4个特征基因表达均逐步升高(图3D、E)。Kaplan-Meier分析进一步证实高风险组预后显著较差(图3F),其1年、3年AUC分别为0.771和0.727(图3I)。该模型在多个外部验证队列中表现一致:ICGC队列中高风险组总生存期更短(图3G),1年、3年AUC为0.791和0.751(图3J);GSE54236与GSE202069队列同样显示高风险组预后较差(图3H),且两个队列的1年、3年AUC均保持较高水平(图3K),进一步证实SIR-PS具有稳健的预测能力。

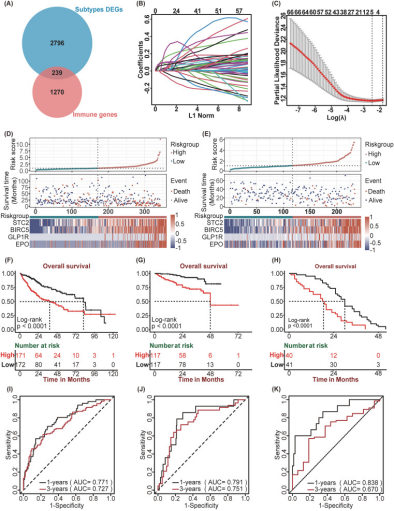
图3
3、 SIR-PS的临床意义与肿瘤微环境探索
为探究SIR-PS与临床病理特征的关系,分析显示高风险组与多个HCC特征显著相关(图4A),具体表现为AFP水平升高、Sub1亚型和女性比例更高、组织学分级更晚、病理分期和T分期更进展。通过CIBERSORT算法分析免疫细胞浸润发现,高风险组记忆B细胞和调节性T细胞等浸润增加,而活化NK细胞等减少(图4B)。同时,高风险组多数免疫检查点基因表达上升(图4B)。在免疫治疗队列中,高风险组患者响应率更高(图4C),风险评分预测治疗响应的AUC达0.787(图4D)。

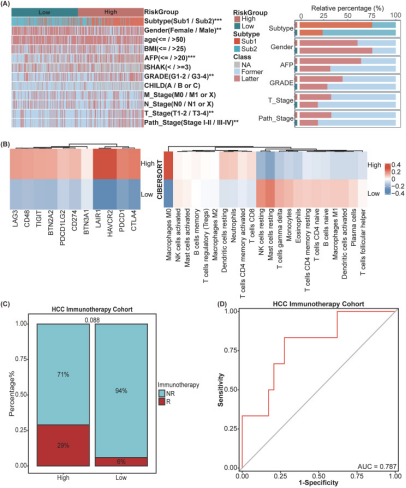
图4
4、SIR-PS的空间转录组分析
首先,分析了低风险组和高风险组中突变频率最-高的10个基因。肿瘤突变图谱显示,在TCGA数据库中,高风险组和低风险组中突变频率最-高的基因分别是TP53(突变频率40%)和CTNNB1(突变频率33%)(图5-A、B)。为确定模型发挥作用的细胞类型,分析了HCC患者的空间转录组数据,结果显示肝癌细胞中的风险评分最-高,表明患者的SIR-PS风险评分主要由这些癌细胞的风险评分决定(图5C),同时STC2和BIRC5主要在肝癌细胞中表达。

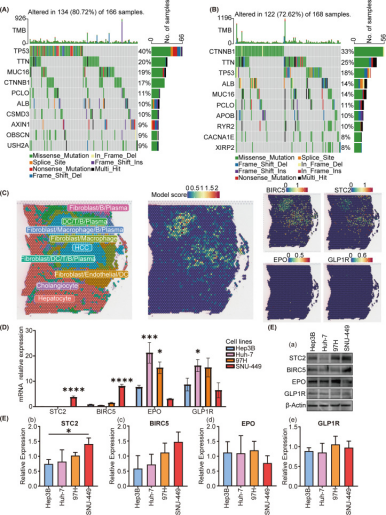
图5
5、HCC细胞系中的qPCR和Western blotting验证
基于空间转录组分析结果,选择SNU-449、97H、Hep3B和Huh7四种HCC细胞系进行细胞水平验证,其中SNU-449和97H细胞系的恶性程度或转移能力高于Hep3B和Huh7细胞系,通常意味着更差的预后。无论是qPCR还是Western blotting检测,STC2和BIRC5在SNU-449和97H细胞系中的表达水平均高于Huh7和Hep3B细胞系(图5D、E),与它们的恶性程度一致,而EPO和GLP1R在mRNA和蛋白质水平上未显示出明显的表达趋势。
6、基于HCC组织芯片IHC染色的SIR-PS验证
基于四个特征基因的预后潜力,对HCC组织芯片进行了IHC染色分析。结果显示,与正常组织相比,STC2、BIRC5、EPO和GLP1R在HCC组织中表达均显著升高(图6A–D)。进一步按IHC评分将患者分为高、低表达组,Kaplan-Meier分析表明,这四种基因高表达患者的预后均显著较差(图6E–H)。

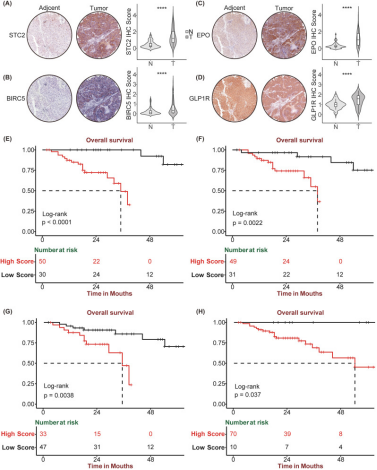
图6
基于上述四基因的IHC评分,我们进一步利用SIR-PS模型计算每位患者的风险评分,并将患者划分为高、低风险组。Kaplan-Meier分析显示,在整个组织芯片队列中,高风险组患者预后显著更差(图7A)。时间-ROC曲线显示,该模型预测1年和3年生存率的AUC值分别为0.711和0.795(图7B)。
作为对比,我们还评估了临床常用标志物GPC3和CK19在同一队列中的预后价值。Kaplan-Meier分析表明,两者高、低表达组间的生存差异均不显著(图7C、E)。其1年和3年AUC值也普遍较低(图7D、F),提示SIR-PS模型在预后预测方面优于传统标志物。

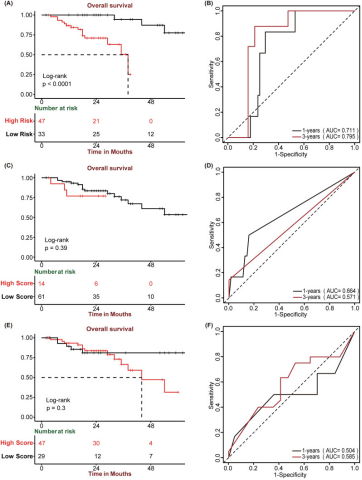
图7
7、预后模型影响免疫治疗效果的机制探索
由于风险评分在接受抗PD1/PDL1治疗的肝癌免疫治疗队列中具有良好的预测效果,SIR-PS可能通过影响PDL1表达来调控免疫治疗efficacy。在TCGA-LIHC队列中,STC2和BIRC5的表达水平及风险评分与PDL1表达水平呈正相关(图8A、B、E、F),表明STC2和BIRC5均能促进癌细胞上PDL1的表达,从而促进肿瘤免疫逃逸,而EPO和GLP1R与PDL1之间无明显相关性(图8C、D)。进一步探索了STC2和BIRC5调控PDL1的潜在机制,由于基因表达可能通过miRNA相互影响,利用MultiMiR包筛选TarBase数据库中经实验验证的、可结合STC2、BIRC5和PDL1的miRNA,共筛选出87个靶向PDL1的miRNA,其中PDL1与STC2共有61个miRNA,PDL1与BIRC5共有48个miRNA(图8G、H、表4)。

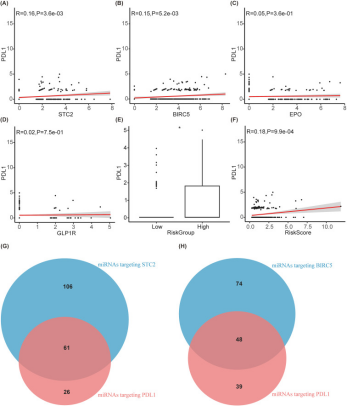
图8




