IF:8.3,网络药理学+转录组+蛋白质组,解析大黄素对食管鳞状细胞癌糖酵解和氧化磷酸化的双重攻击!
题目:靶向肿瘤代谢:大黄素对食管鳞状细胞癌糖酵解和氧化磷酸化的双重攻击
英文名:Targeting tumor metabolism: The dual attack of emodin on glycolysis and oxidative phosphorylation in esophageal squamous cell carcinoma
杂志:Phytomedicine
影响因子:8.3
发表时间:2025年6月8日
研究背景:食管鳞状细胞癌(ESCC)死亡率高且化疗耐药性强,5年生存率仅30.3%。大黄素作为中药活性成分,在结直肠癌、乳腺癌中显示抗癌活性,但在ESCC中的应用及机制尚未明确。
研究思路:通过体外细胞实验(ESCC细胞系)和体内异种移植模型,结合网络药理学、蛋白质组学、Seahorse代谢分析及Western blot等技术,探究大黄素对ESCC的抑制作用,明确其对糖酵解和氧化磷酸化(OXPHOS)的双重抑制效应及p53、FOXO信号通路的介导机制,验证其体内外抗ESCC活性及安全性。
研究结果:
1、大黄素抑制食管鳞状细胞癌细胞增殖
为全面评估大黄素(图1A),处理48小时后,KYSE150、KYSE170、ECA109和KYSE180细胞的IC₅₀值分别为15.64μM、22.75μM、18.80μM和16.81μM(图1B)。与阳性对照药组(20μM5-氟尿嘧啶)相比,5、10和20μM浓度的大黄素产生了显著更强的抑制效果(图1C)。基于这些结果,选择对大黄素敏感性不同的KYSE150和KYSE170细胞进行后续实验。集落形成实验表明,与同等剂量的5-氟尿嘧啶相比,大黄素显著减少了集落数量和大小(图1D)。这些数据表明,大黄素以时间和剂量依赖性方式抑制食管鳞状细胞癌细胞的生长和集落形成。
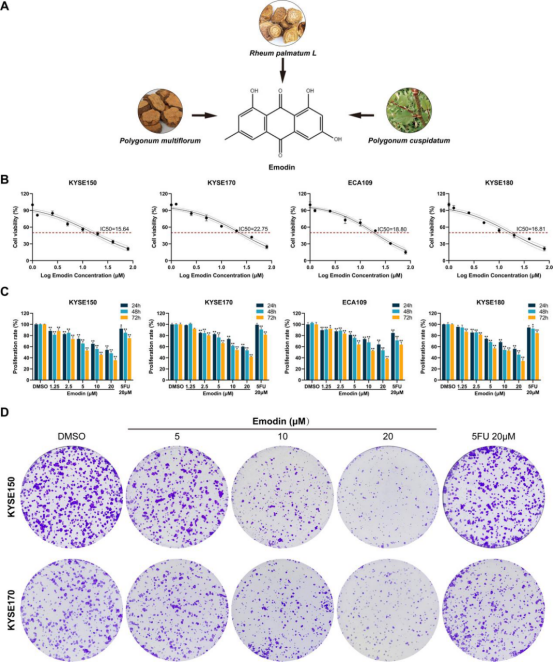

图1
2、大黄素诱导食管鳞状细胞癌细胞凋亡并引发G2/M期细胞周期阻滞
通过流式细胞术评估大黄素对食管鳞状细胞癌细胞的凋亡作用,并阐明其作用机制。分析结果显示,大黄素以剂量依赖性方式显著增加食管鳞状细胞癌细胞的凋亡率(图2A)。值得注意的是,同等剂量下5 - 氟尿嘧啶处理后的凋亡率显著低于大黄素诱导的凋亡率。为进一步证实大黄素的凋亡作用,提取经不同浓度大黄素(5、10和20μM)处理48小时的食管鳞状细胞癌细胞总蛋白并进行蛋白质印迹分析。该实验旨在量化外在凋亡标志物(半胱天冬酶8和裂解型半胱天冬酶8)和内在凋亡标志物(半胱天冬酶9和裂解型半胱天冬酶9)相关蛋白丰度,阐明大黄素诱导的凋亡机制。结果显示,大黄素处理未显著改变半胱天冬酶8和裂解型半胱天冬酶8蛋白水平,但裂解型半胱天冬酶3/9水平呈剂量依赖性升高。 (图2B)。因此,研究结果表明大黄素主要通过内在半胱天冬酶9/半胱天冬酶3通路触发食管鳞状细胞癌细胞凋亡。
通过流式细胞术评估大黄素对食管鳞状细胞癌细胞周期的影响。大黄素以剂量依赖性方式显著增加G2/M期细胞比例,且同等剂量下该比例高于5-氟尿嘧啶处理组(图2C)。大黄素处理可下调食管鳞状细胞癌细胞中周期蛋白B1和CDK1的表达(图2D),这可能导致细胞周期阻滞在G2/M期并促进内在凋亡。
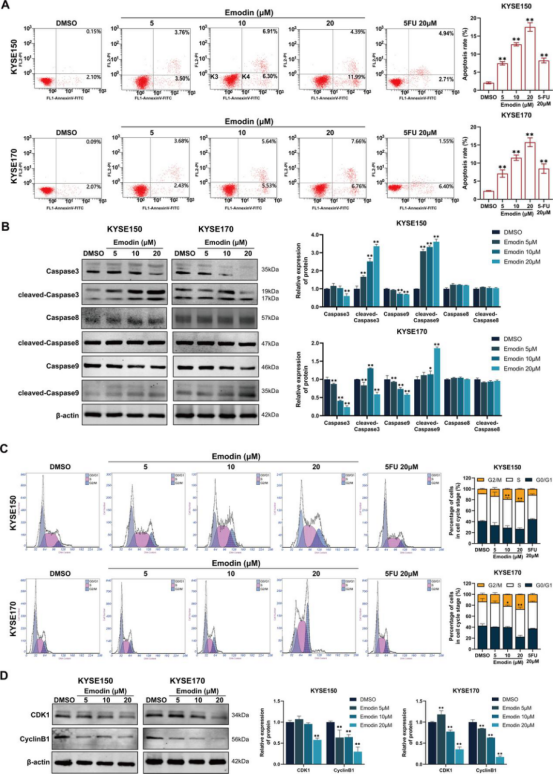

图2
3、网络药理学预测大黄素调控食管鳞状细胞癌的机制
为阐明大黄素对食管鳞状细胞癌作用的分子机制,从PubChem数据库中获取大黄素的三维结构(图3A)。从TCGA数据库中筛选出食管鳞状细胞癌中的差异表达得到41个候选基因(图3B)。通过Cytoscape分析确定TP53、HSP90、CDK1/2和PARP为关键通路中的核心基因(图3C)。基因本体(GO)富集分析表明,在生物学过程层面,细胞周期过程(尤其是与G2/M期相关的过程)最为显著(图3D),KEGG通路显示,这些基因富集于p53和FOXO信号通路(图3E)。大黄素处理可显著增加食管鳞状细胞癌细胞中p53和FOXO3蛋白水平,并降低磷酸化FOXO3(p-FOXO3)蛋白水平(图3F)。

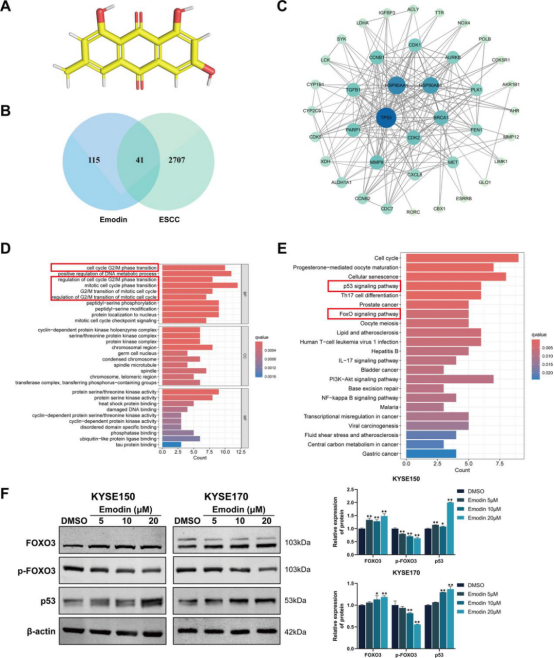
图3
4、大黄素对食管鳞状细胞癌细胞影响的蛋白质组学研究
为进一步阐明大黄素对食管鳞状细胞癌细胞的作用机制,通过高效液相色谱-质谱联用(HPLC-MS)进行蛋白质分析(图4A)。主成分分析(PCA)证实各处理组之间存在明显差异(图4B)。共鉴定出221个显著差异表达的蛋白质,其中大黄素处理后有51个蛋白质上调,170个蛋白质下调(图4C)。GO富集分析表明,大黄素主要影响食管鳞状细胞癌细胞中的糖酵解和细胞呼吸等生物学过程(图4D)。KEGG分析显示,代谢通路(尤其是糖酵解和氧化磷酸化)显著富集(图4E)。基因集富集分析(GSEA)显示,大黄素处理组中糖酵解和氧化磷酸化过程下调(图4F)。在221个差异蛋白中,9个与糖酵解通路相关,13个与氧化磷酸化通路相关(图4G)。实时荧光定量聚合酶链反应(RT-qPCR)证实,大黄素显著下调氧化磷酸化和糖酵解中关键分子的mRNA表达水平。这些结果支持大黄素调控食管鳞状细胞癌细胞能量代谢通路的假设。
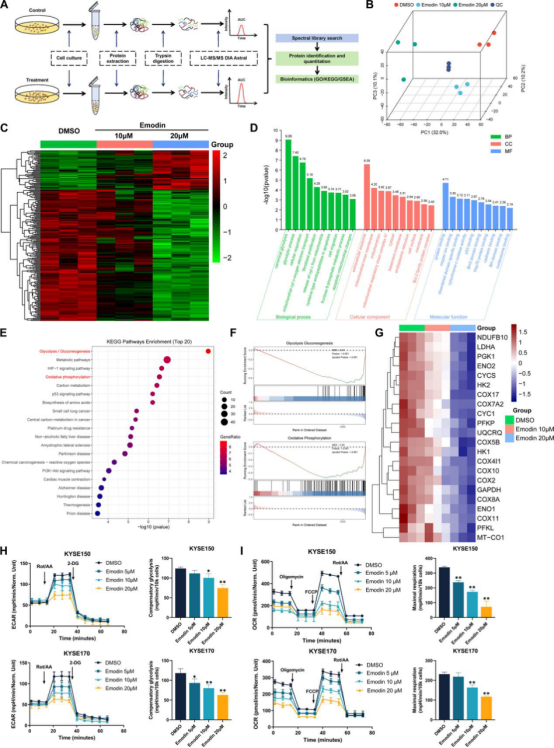

图4
5、大黄素诱导食管鳞状细胞癌细胞代谢重编程
为评估大黄素对食管鳞状细胞癌能量代谢的影响,利用Seahorse平台进行糖酵解速率测定和线粒体应激测试。与对照组相比,糖酵解速率测定数据显示,大黄素处理以剂量依赖性方式降低细胞外酸化率(ECAR)(图4H),表明食管鳞状细胞癌细胞的糖酵解受到抑制。同时,线粒体应激测试结果表明,大黄素可抑制氧化磷酸化,表现为氧消耗率(OCR)呈剂量依赖性降低(图4I)。这些结果表明,大黄素可抑制食管鳞状细胞癌细胞的糖酵解和氧化磷酸化,提示其诱导代谢重编程并阻碍食管鳞状细胞癌进展。
6、抑制p53和FOXO3通路可抵消大黄素靶向糖酵解和氧化磷酸化的作用
通过网络药理学和蛋白质组学研究,提出大黄素通过p53和FOXO信号通路调控食管鳞状细胞癌细胞的糖酵解和氧化磷酸化。为验证这一假设,将食管鳞状细胞癌细胞单独或联合使用p53通路抑制剂PFT-α(20μM)和FOXO通路抑制剂AS1842856(10μM)与大黄素共同处理48小时。流式细胞术分析表明,与对照组相比,大黄素(10μM)显著提高了凋亡率。然而,同时使用大黄素与PFT-α或AS1842856处理的细胞,其凋亡率显著降低,与单独使用抑制剂处理的细胞无显著差异(图5-A)。糖酵解速率测定进一步表明,大黄素(10μM)显著降低糖酵解水平,但联合使用PFT-α或AS1842856可逆转这一效应(图5B)。类似地,线粒体应激测试显示,大黄素处理后氧消耗率显著降低,但联合使用AS1842856可使氧消耗率恢复至与单独使用AS1842856相当的水平。有趣的是,大黄素与PFT-α联合处理进一步降低了氧消耗率(图5C)。总体而言,这些发现表明,p53和FOXO通路是大黄素诱导食管鳞状细胞癌细胞代谢重编程所必需的。
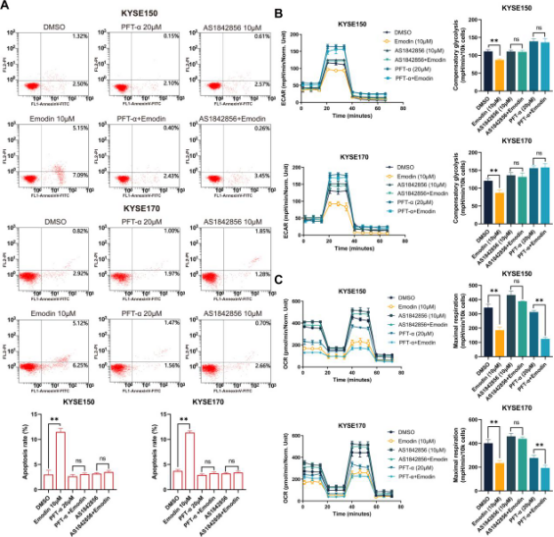

图5
7、大黄素对食管鳞状细胞癌异种移植瘤的抑制作用
为进一步证实大黄素的抗癌作用,将KYSE150细胞接种到BALB/c裸鼠体内构建异种移植模型。实验方案如图6A所示。接种后第7天,将小鼠随机分为对照组、阳性药物组(5-氟尿嘧啶,25mg/kg)和大黄素组(10、25和50mg/kg)。大黄素处理以剂量依赖性方式显著抑制食管鳞状细胞癌异种移植瘤的生长。同等剂量下,大黄素的效果优于5-氟尿嘧啶(图6B)。通过监测体重评估大黄素的安全性,结果显示大黄素组与对照组之间无显著差异(图6C)。大黄素处理以剂量依赖性方式降低肿瘤重量和体积(图6D、6E)。对脾脏、肝脏、心脏、肺和肾脏的组织学分析未发现任何异常病理形态学变化,表明大黄素对这些器官无明显毒性(图6F)。这些发现表明,持续给予大黄素可显著抑制肿瘤生长且无不良反应。苏木精-伊红(H&E)染色显示,大黄素处理组的肿瘤细胞排列较稀疏,呈现松散的凋亡形态,细胞核碎裂(图6F)。肿瘤组织的免疫组织化学(IHC)分析显示,大黄素组中Ki67和p-FOXO3的表达降低,而p53和FOXO3蛋白的表达增加(图6G)。这些体内观察结果与体外研究结果一致,表明大黄素通过p53和FOXO信号通路抑制异种移植瘤的发展。
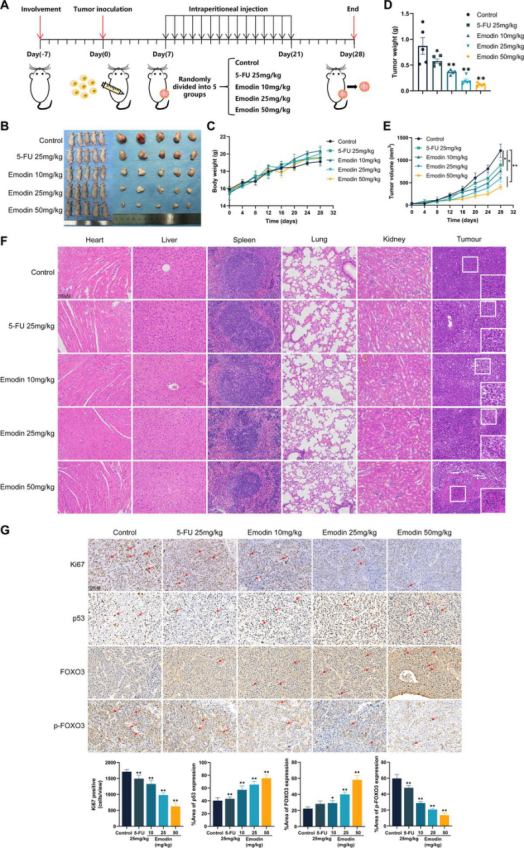

图6
总结:大黄素通过调控p53和FOXO通路,双重抑制ESCC细胞糖酵解与OXPHOS,诱导G2/M期阻滞和内在凋亡,体内外实验均证实其抗ESCC活性且安全性良好,有望成为ESCC治疗候选药物。星生物深耕生信分析十余载,有丰富的实验方案、完善的下游验证、机制研究服务,一对一专属服务为您排忧解难,助您轻松应对毕业和晋升!




